分析下表中各项的排布规律,按此规律排布第26项应为 ( )
| 1 |
2 |
3 |
4 |
5 |
| C2H4 |
C2H6 |
C2H6O |
C2H4O2 |
C3H6 |
| 6 |
7 |
8 |
9 |
10 |
| C3H8 |
C3H8O |
C3H6O2 |
C4H8 |
C4H10 |
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是()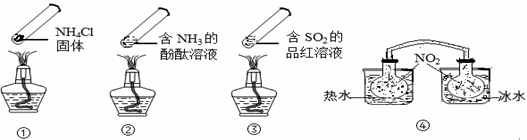
| A.加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,②、③溶液均变红,冷却后又都变为无色 |
| C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D.四个“封管实验”中所发生的化学反应都是可逆反应 |
在离子浓度相同的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是()
| A.在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B.在含AlO2—、SO32—、OH—的溶液中逐滴加入硫酸氢钠溶液:OH—、AlO2—、SO32— |
| C.在含I—、SO32—、Br—的溶液中不断通入氯气:I—、Br—、SO32— |
| D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:Fe3+、NH4+、H+ |
下列各组在溶液中反应,不管反应物的量是多少,都能用同一离子方程式表示的是()
| A.AlCl3与氨水 | B.铁与稀硝酸 |
| C.HCl与Na2CO3 | D.NaHCO3与Ca(OH)2 |
下列离子方程式正确的是()
A.明矾溶液中滴加Ba(OH)2溶液至SO 完全沉淀:Al3++Ba2++SO 完全沉淀:Al3++Ba2++SO +3OH-===BaSO4↓+Al(OH)3↓ +3OH-===BaSO4↓+Al(OH)3↓ |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O |
| C.铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O |
| D.MgSO4溶液与Ba(OH)2溶液混合:SO42-+Ba2+=BaSO4↓ |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象: ①向溶液中滴加足量氯水后,溶液变橙黄色,且有无色气泡冒出②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断:该溶液中肯定不存在的离子组是()
| A.Al3+ Mg2+ I-SO32- | B.Mg2+ Na+ CO32-I- |
| C.Al3+Na+ SO32-I- | D.Na+ CO32- Br-I- |