在25 ℃时,密闭容器中X、Y、Z三种气体的浓度变化情况如图,下列说法错误的是 ( )。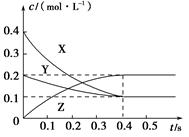
A.反应可表示为3X+Y 2Z 2Z |
| B.从反应开始到0.4 s时,以Y表示的化学反应速率为0.25 mol·L-1·s-1 |
| C.增大压强使平衡向生成Z的方向移动,正逆反应速率均增大 |
| D.升高温度,平衡常数一定增大 |
实现Al3++3AlO2-+6H2O=4Al(OH)3↓,正确的做法是
| A.向铝盐溶液中不断加入纯碱溶液 | B.向铝盐溶液中不断加入小苏打溶液 |
| C.向烧碱溶液中不断滴入铝盐溶液 | D.向铝盐溶液中不断滴入烧碱溶液 |
下列叙述正确的是
| A.发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B.金属阳离子被还原后,一定得到该元素的单质 |
| C.核外电子总数相同的原子,一定是同种元素的原子 |
| D.能与酸反应的氧化物,一定是碱性氧化物 |
X、Y、Z、W有如图所示的转化关系,则X、Y可能是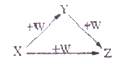
①C、CO②AlCl3、Al(OH)3③Fe、Fe(NO3)2④Na2CO3、NaHCO3
A.①②③④ B.①② C.③④ D.①③
向含有FeCl2、FeCl3、AlCl3、NH4Cl的混合溶液中先加入过量Na2O2固体,微热搅拌后再加入过量盐酸,溶液中阳离子数目变化最小的是
| A.Fe2+ | B.Fe3+ | C.Al3+ | D.NH4+ |
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平,下图表示了三种金属被人类开发利用的大致年代,之所以有先后,主要取决于
| A.金属的导电性强弱 | B.金属在地壳中的含量多少 |
| C.金属的化合价高低 | D.金属的活动性大小 |