下图中A~J分别代表相关反应的一种物质。已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出。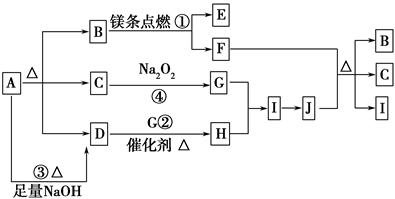
已知:2Mg+CO2 2MgO+C,请填写以下空白:
2MgO+C,请填写以下空白:
(1)A的化学式________。
(2)写出反应②的化学方程式:________________________________________。
(3)写出反应③的离子方程式:________________________________________。
(4)J与F反应的化学方程式:_________________________________________。
(5)在反应④中,当生成标准状况下2.24 L G时,转移电子数为________ mol。
(8分)俗话说“民以食为天”,食物是人类赖以生存的物质基础。
| 主食 |
副食 |
饮料 |
| 米饭 |
烧豆腐、红烧鱼、三层肉 |
牛奶 |
上表是小明制定的食谱,在食谱中含有的营养素主要有,,。小明制订的食谱中还缺乏的一种营养素是。
用铝制饭盒盛放醋酸,一段时间后,饭盒被腐蚀,该种腐蚀属,反应的电极反应式为。若用铝制饭盒盛放食盐(含水时),一段时间后,饭盒被腐蚀,这种腐蚀叫做,反应原理是(写电极反应式)。
(6分)四种短周期元素的微粒信息如下表:
| 元素代号 |
Q |
R |
X |
Z |
| 微粒信息 |
离子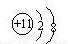 |
单质分子R2 |
离子:X3+ |
一种原子816Z |
已知Q、R、X在同一周期,R2在常温常压下为气态。完成下列填空:
(1)Q位于周期表第----周期----族。化合物Q2Z的电子式为(元素符号表示)
(2)Q、R、X的原子半径由大到小的顺序为。Q、R、X、Z中金属性最强的是(元素符号表示)
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的离子方程式为
(1)用惰性电极电解饱和NaCl溶液,请写出:
① 阳极的电极反应为:;
总反应离子方程式:。
② 要使电解后的溶液恢复到和原溶液一样,则应加入一定量的。
(2)用电解法精炼粗铜,电解液选用CuSO4溶液。请回答:
① 阳极的电极材料是,电极反应式是;
② 阴极电极的材料是,电极反应式是。(杂质发生的电极反应不必写出)
由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式。若1 g水蒸气转化为液态水放热2.444 kJ,则反应H2(g) + 1/2 O2(g) = H2O(l)的△H = kJ·mol-1。