硫酸、盐酸、硝酸是工业上常用的三种酸
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性;
(2)对于硫酸而言,溶质的质量分数越大,溶液的酸性越强。常温下,10%的稀硫酸的pH______(填“大于”“小于”或“等于”)2%的稀硫酸的pH;
(3)如果要使稀硫酸的pH升高。你采取的化学反应的方法有(要求所选的物质类别不同): ______________;_______________;
(4)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
请结合下图回答问题:
(1)写出有标号的仪器名称:①,②。
(2)实验室用高锰酸钾制取O2的化学方程式为,用A、D装置制取O2时,为防止高锰酸钾进入导管,可采取的措施是。
(3)实验室用B、C装置制取CO2的化学方程式为,若将发生装置由B改为F,其优点是。
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水。SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气。用下图所示装置收集一瓶干燥的SO2,装置中导管按气流方向连接顺序是①→②→→→⑤(填序号);图中漏斗的作用是;烧杯中NaOH溶液的(用化学方程式表示)。
新制
与肼(
)反应可制备纳米级
,同时放出
,向红色的
固体中加入过量稀盐酸,溶液由无色变为蓝绿色,容器底部仍有红色固体。
(1)生成
反应的化学方程式中,
的化学计量数为2,其化学方程式为;
(2)溶液由无色变为蓝绿色反应的化学方程式为。
根据下列实验装置回答问题:
(1)图①相当于化学实验中的装置;
(2)图②实验中观察到的明显现象是;
(3)图③电池工作时反应的化学方程式为,溶液
(填"变大"或"变小")。
仔细观察下图实验,回答下列问题: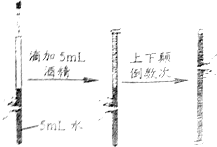
(1)水与酒精混合后,总体积
(填"大于"、"等于"、"小于")。
(2)该实验说明。
请从下列物质中选择适当的物质填空(填字母编号):
| A. | 聚乙烯 | B. | 活性炭 | C. | 石灰石 | D. | 浓硫酸 |
E.蛋白质 F.肥皂水 G.硝酸钾 H.硝酸铵
(1)用于食品包装;(2)可作复合肥料;
(3)用于冰箱除异味;(4)溶于水能放热;
(5)用于工业炼铁;(6)鱼、虾中富含。