合成氨工业中,原料气(N2、H2、混有少量CO、NH3)在进入合成塔之前,常用醋酸二氨合铜(Ⅰ)溶液来吸收CO,其反应为CH3COO[Cu(NH3)2]+CO+NH3
CH3COO[Cu(NH3)3]·CO(正反应为放热反应)。
(1)必须除去CO的原因是___________________________。
(2)醋酸二氨合铜(Ⅰ)溶液吸收原料气中CO的适宜条件是______________________。
(3)吸收CO后的醋酸铜(Ⅰ)氨溶液经适当处理又可再生,恢复其吸收CO的能力而循环使用,其再生的条件是______________________________。
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系。回答下列问题:
(1) 若X基态原子外围电子排布式为3s2,甲是由第二周期两种元素的原子构成的气态化合物分子, Y基态原子的轨道表示式为,甲的电子式为
(2)若X原子的价电子排布为ns(n-1)np(n+2),常温下Y为易挥发的液体物质、乙为无色易溶于水的气体。则Z为,组成Y的元素的基态原子的电子排布式为。
(3)若X、Y均为金属单质,X基态原子外围电子排布式为3s23p1,甲为具有磁性的黑色固体,则X与甲反应的化学方程式为:,Y2+离子的电子排布式为。
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 |
A |
B |
C |
D |
| 性质结构信息 |
原子中最外层电子数为电子层数的2倍。常温下为淡黄色固体,其燃烧热为Q KJ/mol |
单质常温、常压下是气体,能溶于水。原子的M层p轨道有1个未成对的电子 |
单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰。 |
原子最外层电子层上s电子数等于p电子数。单质是一种重要的半导体材料。 |
(1)写出A的燃烧热方程式。
(2)写出B单质与水反应的化学方程式。
(3)电解B与C的化合物水溶液是重要化学工艺,写出离子方程式。
(4)A与C形成的化合物存在的化学键为(填“共价键”或“离子键”)。
(5)A、B、D三种元素电负性由小到大的顺序为(写元素符号)。
(6)B、D两元素非金属性较弱的是(写元素符号)。请设计一个实验证明这一结论:。
下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 1 |
① |
|||||||
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|||
| 4 |
⑩ |
(1)写由上述元素组成的分子中电子总数为10的分子(至少两种):。
(2)比较:②、③、④、⑤的第一电离能:>>>(写元素符号)。
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是;碱性最强的化合物的电子式是:
(4)具有两性的最高价氧化物是(填化学式);写出其与氢氧化钠溶液反应的离子方程式:。
(5)下表为原子序数依次增大的短周期元素A~E的第一到第五电离能数据。
| 电离能I(eV) |
A |
B |
C |
D |
E |
| I1 |
11.3 |
13.6 |
5.2 |
7.6 |
6.0 |
| I2 |
24.4 |
35.1 |
49.3 |
15.0 |
18.8 |
| I3 |
47.9 |
54.9 |
71.6 |
80.1 |
28.4 |
| I4 |
64.5 |
77.4 |
98.9 |
109.2 |
112.0 |
| I5 |
392.1 |
113.9 |
138.3 |
141.3 |
153.7 |
试回答:表中可能为非金属元素的是(填字母);若D、E为同周期相邻元素,表中D比E的第一电离能略大,其原因是 。
A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为;
(2)B元素的负一价离子的电子层结构都与氩相同,B的原子结构示意图为
(3)C元素是第三周期中无未成对电子的主族元素,它的轨道排布式为;
(4)D元素基态原子的M层全充满,N层只有一个未成对电子,D基态原子的电子排布式为
(5)E原子共有3个价电子,其中一个价电子位于第三能层d轨道,指出该元素在周期表中所处的周期数和族序数
下图1是工业上“碱法烟气脱硫法” 示意图,下图2是工业上“石灰→石膏烟气脱硫法”示意图,回答: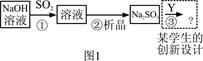

已知:
| 试剂 |
Ca(OH)2 |
NaOH |
| 价格(元/kg) |
0.36 |
2.9 |
| 吸收SO2的成本(元/mol) |
0.027 |
0.232 |
(1)图1中,反应①的离子方程式为,之一是。
(2)图2中,反应⑤的目的是稳定固化硫元素形成高价态的化合物,氧气的作用是。该法的优点之一是。
(3)“碱法烟气脱硫法”中的产物Na2SO3的稳定性不好,易使硫元素重新转化为挥发性污染物,为避免之,设计了③的反应,写出其化学方程式为。