下列有机物系统命名正确的是( )
A.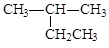 2-乙基丙烷 2-乙基丙烷 |
| B.CH3CH2CH2CH2OH 1-丁醇 |
C.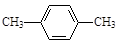 对二甲苯 对二甲苯 |
D.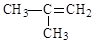 2-甲基-2-丙烯 2-甲基-2-丙烯 |
下列分子的电子式书写正确的是
A.氨气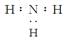 |
B.四氯化碳 |
C.氮气 |
D.二氧化碳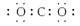 |
随着人们对物质组成研究的深入,物质的分类也更加多样化。下列说法正确的是
| A.Na2O2、Al2O3、Fe2O3都是碱性氧化物 |
| B.CH3COOH、NH3·H2O、HClO都是弱电解质 |
| C.磁铁矿、铝土矿、绿矾都是混合物 |
| D.烧碱、纯碱、熟石灰都是碱 |
我国成功发射了“嫦娥一号”月球探测卫星。人类探测月球发现,其土壤中存在较丰富的质量数为3的氦元素,它可以作为核聚变的重要原料之一。以下关于3He的说法正确的是
| A.是4He的同分异构体 | B.比4He多一个中子 |
| C.是4He的同位素 | D.比4He少一个质子 |
某溶液中含有大量的Cl-、CO32-、OH-等三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作中,顺序正确的是
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
| A.①②④②③ | B.④②①②③ | C.①②③②④ | D.④②③②① |
实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律的摆放在实验桌上,如下图。做“硫酸的性质”的实验时,某同学取用BaCl2溶液后,应把它放回的位置是