某金属氧化物在光照下可生成具有很强氧化能力的物质,能用来消除空气或水体中的污染物。下列有关该金属氧化物应用的叙述不正确的是( )。
| A.将形成酸雨的SO2氧化为SO3 |
| B.将家居装修挥发出的甲醛氧化为CO2和H2O |
| C.将医药废水中的苯酚氧化成H2O和CO2 |
| D.将电镀废水中的氰根离子CN-氧化成CO2和N2 |
将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
| A.最终得到7.8g的沉淀 |
| B.反应过程中得到6.72L(标准状况)的气体 |
| C.最终得到的溶液中c(NaCl)=1.5mo/L |
| D.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-) |
下列除杂质的操作中不正确的是
| A.铁粉中混有铝粉:加入过量烧碱溶液充分反应后过滤 |
| B.FeCl2溶液中混有FeCl3:加入过量铜粉充分反应后过滤 |
| C.Na2CO3固体中混有少量NaHCO3:加入适量NaOH溶液 |
| D.Al(OH)3中混有Mg(OH)2:加入足量烧碱溶液后过滤,向滤液中通入过量CO2后过滤 |
将1 mol 含镁物质的量分数为a的镁铝合金溶于含有b mol HNO3的稀溶液中,刚好完全反应,NO为唯一还原产物。向所得溶液中逐滴加入NaOH溶液至沉淀不再减少为止,将所得沉淀过滤、洗净、灼烧至恒重,所得固体质量与原合金质量相等。下列说法中正确的是
①合金含镁质量分数为60%②反应中放出气体体积在标准状况下为(1-a/3)× 22.4 L③反应过程中最大沉淀质量为(78-20a)g④反应中共消耗NaOH[b-(1-a/3)]mol
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的10 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
| A.该反应显示硫酸具有酸性 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.反应中硫酸作氧化剂 |
下列各组物质中,满足下图物质一步转化关系的选项是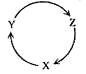
| 选项 |
X |
Y |
Z |
| A |
NO |
NO2 |
HNO3 |
| B |
Cu |
CuSO4 |
Cu(OH)2 |
| C |
C |
CO |
CO2 |
| D |
Si |
SiO2 |
H2SiO3 |