一定温度下,在一体积固定的密闭容器中加入2 mol X和1 mol Y,发生如下反应:2X(g)+Y(g) aZ(g)+W(g) ΔH=-Q kJ·mol-1(Q>0,a是正整数)。当反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;平衡后混合气体的平均相对分子质量与温度的关系如图所示,下列说法不正确的是( )
aZ(g)+W(g) ΔH=-Q kJ·mol-1(Q>0,a是正整数)。当反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;平衡后混合气体的平均相对分子质量与温度的关系如图所示,下列说法不正确的是( )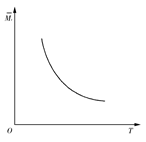
| A.温度升高,平衡常数K减小 |
| B.化学计量数a为1 |
| C.维持温度不变,若起始时向容器中加入a mol Z、1 mol W反应达到平衡后放出的热量为Q2 kJ,则Q1+Q2=Q且Q>Q1>Q2 |
| D.X的转化率α=Q1/Q |
下列说法中错误的是
| A.推广使用新能源,可以减少二氧化碳等温室气体的排放 |
| B.发电厂的燃煤在燃烧时加入适量石灰石,可减少二氧化硫排放 |
| C.石油、煤、天然气均属于可再生的化石燃料 |
| D.太阳能、氢能、风能属于清洁能源 |
以下离子方程式书写错误的是( )
①铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
②硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
③碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑
④氢氧化铜中加入盐酸:OH-+H+=H2O
| A.①②④ | B.①③ | C.全部 | D.①④ |
9.2 g金属钠投入到足量的重水中,则产生的气体中含有( )
| A.0.2 mol中子 | B.0.4 mol电子 | C.0.2 mol质子 | D.0.4 mol分子 |
将0.4 g NaOH和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2物质的量的关系是( )
某溶液中阳离子只含K+,其中Cl-、Br-、I-的个数比为1∶2∶3,欲使这些离子个数比变为3∶2∶1,需要通入的氯分子与原溶液中I-的个数比应为( )
| A.1∶2 | B.2∶1 | C.1∶3 | D.3∶1 |