某温度下,CO2饱和溶液的浓度是0.03mol/L,其中1/3的CO2转变为H2CO3,而H2CO3仅有0.1%发生如下电离:H2CO3 H++HCO3—,则溶液的pH约为( )
H++HCO3—,则溶液的pH约为( )
| A.3 | B.4 | C.5 | D.6 |
下列叙述正确的是
①离子化合物中不一定含有金属阳离子②分子晶体中不一定含有共价键
③有机物中不一定都含有氢元素④酸酐都能直接与水反应生成相应的酸
⑤酸与碱混合都只发生中和反应⑥酸式盐溶于水得到的溶液都显酸性
| A.只有①② | B.只有①②③ |
| C.只有③⑤⑥ | D.只有①②④⑥ |
将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是
A.可以收集到氯气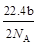 L L |
B.反应后溶液中的Cl―数目为: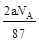 |
C.NA可表示为: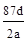 |
D.反应后溶液中的H+数目为: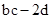 |
在中学化学实验室经常用到下列实验装置,其中不可用于物质分离的装置是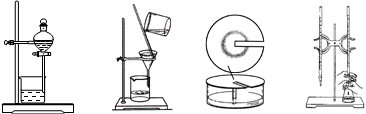
A. B. C. D.
关于晶体的叙述中,正确的是
| A.原子晶体中,共价键的键能越大,熔、沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔、沸点越高 |
| D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
有关生活中常见的有机物的说法正确的是
| A.汽油、苯、乙醇都属于烃类物质 |
| B.油脂皂化后可用盐析的方法使高级脂肪酸钠和甘油分离 |
| C.乙醇能被氧化成乙酸,两者都能与氢氧化钠溶液反应 |
| D.煤的干馏可得煤油,甲烷、乙烯和苯能从石油分馏得到 |