如图所示,横坐标为溶液的pH值,纵坐标为Zn2+离子或Zn(OH)42—离子物质的量浓度的对数,回答下列问题。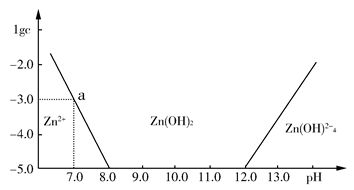
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:________。
(2)从图中数据计算可得Zn(OH)2的溶度积(Ksp)=________。
(3)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围是________________________。
(4)已知:往ZnCl2溶液中加入硝酸铅或醋酸铅溶液可以制得PbCl2白色晶体;25℃时,PbCl2固体在盐酸中的溶解度如下:
| c(HCl)/( mol·L-1) |
0.50 |
1.00 |
2.04 |
2.90 |
4.02 |
5.16 |
5.78 |
| c(PbCl2)/( mol·L-1)×10-3 |
5.10 |
4.91 |
5.21 |
5.90 |
7.48 |
10.81 |
14.01 |
根据上表数据判断下列说法正确的是________(填字母序号)。
A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大
B.PbCl2固体在0.50 mol·L-1盐酸中的溶解度小于在纯水中的溶解度
C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(如配合离子)
D.PbCl2固体可溶于饱和食盐水
(1)①现有11g由 和
和 组成的水分子的物质的量mol,其中含中子数为mol,电子数为个。
组成的水分子的物质的量mol,其中含中子数为mol,电子数为个。
②请画出 2-微粒的结构示意图:。
2-微粒的结构示意图:。
(2)质量相等的两种物质SO2和SO3,两种物质中硫元素质量之比为,分子物质的量之比为,所含氧原子个数之比为。
(3)0.2L 0.5mol/L Al2(SO4)3溶液和0.5L 0.5mol/L Al2(SO4)3溶液所含SO42—离子浓度之比为____________,SO42—离子数目之比为____________。
(4)20.6g NaR 含有Na+0.2mol,则NaR的摩尔质量为,则含R 8.0g 的NaR的物质的量为mol 。
(5)实验室用二氧化锰与浓盐酸反应制取氯气,反应方程式如下:
MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有mol HCl被氧化,转移电子的物质的量为mol,产生的Cl 2在标准状况下的体积为L。
MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有mol HCl被氧化,转移电子的物质的量为mol,产生的Cl 2在标准状况下的体积为L。
有以下几种物质 ①碳酸氢钠晶体;②液态氯化氢;③铁;④蔗糖;⑤乙醇;⑥熔融的K2SO4;⑦干冰;⑧石墨;⑨氨气。填空回答:(填序号)
(1)以上物质能导电的是 。
(2)以上物质中属于电解质的是 。
(3)以上物质中属于非电解质的是 。
(4)以上物质中溶于水后水溶液能导电的是。
(5)分别写出物质①、⑥在水溶液中的电离方程式。
选择下列物质分离和检验方法,将其选项填在横线上。
| A.萃取; | B.升华; | C.结晶; | D.分液;E.蒸馏;F.层析;G.过滤 |
(1)分离饱和食盐水与沙子的混合物。
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)分离水和汽油的混合物。
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)两种互溶液体。
(Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题: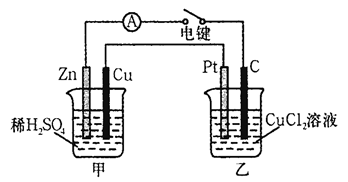
(1)甲装置的名称是____________ (填“原电池”或“电解池”)。
(2) 写出电极反应式: Pt极; 当甲中产生0.1 mol气体时,乙中析出铜的质量应为______________。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色___________(填“变深”、“变浅”或“无变化”)。
(Ⅱ)燃料电池是燃料(如CO、H2、CH4等)跟O2(或空气)反应,将化学能转化为电能的装置。对于以强碱为电解质的CH4燃料电池,负极电极反应式为:,随着放电的进行,溶液的pH(填“变大”“变小”或“不变”)。
(Ⅲ)由Cu2+、Cl-、Na+、SO42-四种离子中的两种离子组成的电解质溶液若干种,可选用铜电极、铂电极进行电解实验。
(1)要使电解过程中溶质的组成和质量不变,而该稀溶液的浓度增大,又无浑浊,应以_______为阳极电解溶液,阳极电极反应式为 。
(2)以铂作阳极电解溶液时,溶液的碱性有明显增强,且溶液保澄清,电解的总反应式为。
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g);ΔH
CH3OH(g);ΔH
(1)已知,该反应在300℃,5MPa条件下能自发进行,则ΔH0,△S0(填“<,>或=”)。
(2)在300℃,5MPa条件下,将0.20mol的 CO与0.58mol H2的混合气体充入2L密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示。
①在0~2min内,以H2表示的平均反应速率为mol·L-1·s-1 ,CO的转化率为。
②列式计算300℃时该反应的平衡常数K=。
③300℃时,将0.50mol CO、1.00mol H2和1.00 mol CH3OH充入容积为2L的密闭容器中,此时反应将。
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
④下列措施可增加甲醇产率的是。
A.压缩容器体积 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H2
(3)若其它条件不变,使反应在500℃下进行,在图中作出甲醇的物质的量浓度随时间的变化的示意图。