A、B、C、D、E、F和G都是有机化合物,它们的关系如图所示: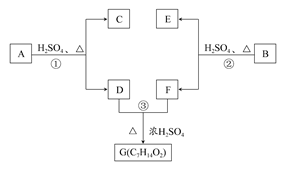
(1)化合物C的分子式是C7H8O,C遇FeCl3溶液显紫色,C的苯环上的一溴代物只有两种,则C的结构简式为 ;
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO3反应放出CO2,则D的分子式为 ,D具有的官能团名称是 ;
(3)反应①的化学方程式是 ;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和F,F可能的结构简式是 ;
(5)E可能的结构简式是 。
(1)X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸盐溶液中,Y表面有Z析出。其活泼顺序是_________________;
(2)由氢气和氧气反应生成1mol水蒸气放热241.8 kJ,写出该反应的热化学方程式:__________________________________。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g) + O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有(填字母)
| A.升高温度 | B.降低温度 | C.增大压强 | D.减小压强 |
E、加入催化剂 G、移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是。
酸雨的形成主要是由于空气中含有气体。现取一份雨水,每隔一段时间测定其pH,结果如下:
| 测定时间/h |
0 |
1 |
2 |
4 |
8 |
| 雨水pH |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
产生上述结果的原因是。
工业上用接触法制取硫酸过程中,硫铁矿在沸腾炉中燃烧的化学方程式是,该反应中氧化剂是______,还原剂是______,被氧化的元素是______,被还原的元素是______。
你认为减少酸雨产生的途径可采取的措施是:①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源(填写标号)______。