原子结构决定元素的性质,下列说法中,正确的是
| A.Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小 |
| B.在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的其沸点也一定最高 |
| C.第2周期元素的最高正化合价都等于其原子的最外层电子数 |
| D.非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 |
下列说法正确的是
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是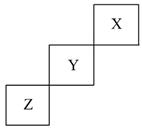
| A.X、Y、Z三种元素中,X的非金属性最强 |
| B.Y的氢化物的稳定性比Z的弱 |
| C.Y的最高正化合价为+7 |
| D.X的单质的熔点比Z的低 |
将4 mol A 气体和2 mol B 气体在2 L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)  2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是
2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是
①用物质A表示的反应的平均速率为0.3 mol/(L·s)
②用物质B表示的反应的平均速率为0.6 mol/(L·s)
③反应达到平衡时,A、B、C的反应速率一定相等
④反应达到平衡时,A、B、C的物质的量均不再变化
A、①③ B、①④ C、②③ D、③④
下列说法中正确的是
| A.物质发生化学反应都伴随着能量变化。 |
| B.伴有能量变化的物质变化都是化学变化。 |
| C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量有可能相同。 |
| D.如果旧化学键断裂吸收的能量大于新化学键形成释放的能量,则该反应为放热反应。 |
下列反应属于氧化还原反应,且△H>0的是
| A.Ba(OH)2·8H2O与NH4Cl反应 | B.灼热的炭与CO2反应 |
| C.铝片与稀H2SO4反应 | D.甲烷在O2中的燃烧反应 |