铁及其化合物应用广泛。
(1)三氯化铁是一种水处理剂,工业制备无水三氯化铁固体的部分流程如下图: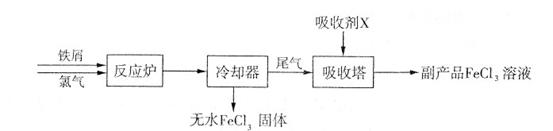
①检验副产品中含有X时,选用的试剂是 (填下列各项中序号)。
a.NaOH溶液 b.KSCN溶液 c.酸性KMnO4溶液 d、铁粉
②在吸收塔中,生成副产品FeCl。的离子方程式为
(2)高铁酸钾(K2FeO4)也是一种优良的水处理剂,工业上,可用铁作阳极,电解KOH溶液制备高铁酸钾。电解过程中,阳极的电极反应式为 ;电解一段时间后,若阳极质量减少28 g,则在此过程中,阴极析出的气体在标准状况下的体积为 L。
(3)硫化亚铁常用于工业废水的处理。
①你认为,能否用硫化亚铁处理含Cd2+的工业废水? (填“能”或“否”)。请根据沉淀溶解平衡的原理解释你的观点(用必要的文字和离子方程式说明): (已知:25℃时,溶度积常数Ksp(FeS)=6.310-18、Ksp(CdS)=3.610-29)
②工业上处理含Cd2+废水还可以采用加碳酸钠的方法,反应如下:2Cd2++2CO32-+H2O=Cd2(OH)2CO3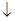 +A。则A的化学式为 。
+A。则A的化学式为 。
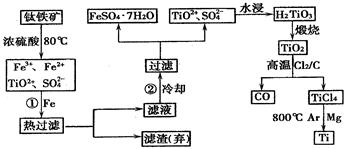
(1) Fe的原子序数为26,Fe位于元素周期表中第周期,第族
(2) 步骤①加铁粉的目的是
步骤②冷却的目的是
(3) 上述过程中,可以利用的副产物是
(4) 写出TiO2、Cl2、C在高温下发生反应的化学方程式
(5) 反应TiCl4+2Mg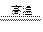 2MgCl2+Ti ,在Ar气体中进行的目的是
2MgCl2+Ti ,在Ar气体中进行的目的是
常温常压下,A、B、C、D均为气体。A与B可发生可逆反应:A+B C+nD。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在不同条件下达平衡时C的浓度如下:
C+nD。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在不同条件下达平衡时C的浓度如下:
| 温度/℃ |
压强/Pa |
C平衡浓度/mol·L-1 |
| 25 |
1×105 |
1.0 |
| 25 |
2×105 |
1.8 |
| 25 |
3×105 |
3.2 |
| 25 |
4×105 |
6.0 |
(1)该可逆反应中化学计量数n的取值范围为__________,理由是______________。
(2)在5×105 Pa时,D的状态为______________。
在763 K和3.04×104kPa时,用CO与H2合成CH3OH:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)设起始时,n(H2)∶n(CO)=m,平衡时CO转化率为α,CH3OH的体积分数为y,则m、α、y三者的关系是___________。
(2)将下表已知数据代入上述关系,进行计算,将结果填入表中:
| m |
α |
y |
| 1 |
0.25 |
① |
| 2 |
0.45 |
② |
| 3 |
③ |
19.35% |
(3)根据表中数据,可得出最佳反应物的配比m是_________,原因是______________。
在某条件下,容器中有如下平衡反应:A+4B 2C+D,正反应为放热反应。此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
2C+D,正反应为放热反应。此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
(1)改变a的取值,再通过改变反应条件,可以使反应重新达到平衡。并限定达到新的平衡时,D的物质的量只允许在d/2到2d之间变化,则a的取值范围应是_______(用a和d的关系式表示)。
(2)如果要使本反应重新建立的平衡中,D的物质的量只允许在d到2d之间取值,则应该采取的措施是_______(从下列给出的选项中选择)。
A.升高反应温度
B.增大反应容器内的压强
C.增大反应容器的容积
D.降低反应温度
E.减小反应容器内的压强
F.减小反应容器的容积
气态可逆反应:mA(g)+nB(g) pC(g)+qD(g),符合图2-31。
pC(g)+qD(g),符合图2-31。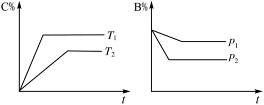
图2-31
试用“>”或“<”填(1)~(4)题。
(1)温度T1_________T2。
(2)压强p1_________p2。
(3)m+n_________p+q。
(4)正反应为________(填“放热”或“吸热”)反应。