现有生活中的下列物质,请回答有关问题:

(1)纯碱属 类(填“酸”“碱”或“盐”),其水溶液的pH 7(填“大于”“小于”或“等于”);
(2)上述物质中含碳酸钙的是 (填序号);
(3)发酵粉的主要成分是(填化学式) ;
(4)上述四种物质(或其中的主要成分)共同的化学性质是都能跟 反应;
(5)工业上可利用上述物质中的 溶液(填溶质化学名称)与石灰水反应制取氢氧化钠,有关反应的化学方程式为 。
化学与生活息息相关,如图为氯化钠注射液的标签说明。请结合标签说明回答下列问题:
(1)氯化钠属于 (填“酸”、“碱”或“盐”)类;
(2)若要配制1000mL该氯化钠注射液需称取 克氯化钠,称量时氯化钠固体应放在托盘天平的 (填“左盘”或“右盘”)上。

请用下列物质的序号填空:
①石墨 ②硝酸钾 ③硫酸铵 ④小苏打 ⑤烧碱
(1)属于复合肥料的是 ;
(2)具有良好导电性,可作电极材料的是 ;
(3)可用于治疗胃酸过多的是 。
请用化学用语填空:
(1)地壳中含量最多的元素是 (填元素符号);
(2)空气中含量最多的物质是 (填化学式)。
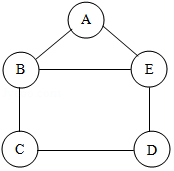
某化学兴趣小组用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应,其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一。
(1)A物质的俗称是 ,E物质的用途是 ;
(2)B与C反应的化学方程式为 。E与D反应的基本类型是 。
(3)按游戏规则,下列能替代B物质的是 (填序号)。
①银 ②氯化铁 ③氯化钡 ④氧化铜
根据表中内容回答下列问题。
|
温度/℃ 溶解度/g 物质 |
0 |
20 |
40 |
60 |
80 |
|
KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
|
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
|
Ca(OH)2 |
0.173 |
0.165 |
0.121 |
0.116 |
0.094 |
(1)随温度升高,Ca(OH)2溶解度的变化趋势是 (填“增大”、“减小”或“不变”)。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是 。
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时存在如图1所示的实验现象,烧杯b中溶解的物质是 ;烧杯a所得溶液溶质的质量分数是 (结果精确到1%),若要使其溶质质量分数增大可采用的方法是 。
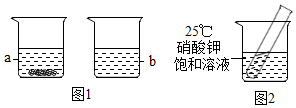
(4)如图2所示,若向烧杯中加入足量的硝酸铵固体并使之充分溶解,在试管中可观察到的现象是 。