煤是一种化石燃料,用煤作燃料生成的SO2气体会造成环境污染。有一种煤每燃烧1 t就会释放出53.3 kg SO2。如果将产生的SO2用熟石灰来完全吸收,其反应的化学方程式为:SO2+Ca(OH)2=CaSO3+H2O,那么燃烧5 t这种煤产生的SO2在理论上需用多少千克的Ca(OH)2来吸收(计算结果取整数)?
磷酸氢二铵[(NH4)2HPO4]是一种复合肥料,能同时均匀地供给农作物养分,充分发挥营养元素间的相互作用。请回答:
(1)磷酸氢二铵分子中氮、氢、磷、氧原子的个数比 。
(2)磷酸氢二铵中氮元素、氢元素、磷元素、氧元素的质量比 。
某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入92.0g稀硫酸,恰好完全反应后,过滤,所得滤液质量为100.0g。
(1)所取样品中铜的质量为 。
(2)从反应后所得的100.0g滤液中取出10.0g溶液,将其稀释为10%的溶液,需要加水多少克?
为测定某黄铜(铜锌合金)样品中铜的含量,某化学活动小组分三次进行实验,实验数据如表,请回答下列问题:
|
所取药品 |
第一次 |
第二次 |
第三次 |
|
黄铜样品质量(g) |
12 |
10 |
10 |
|
稀盐酸质量(g) |
100 |
100 |
150 |
|
生成气体质量(g) |
0.2 |
0.2 |
0.2 |
(1)第 次实验中,药品成分恰好完全反应。
(2)黄铜样品中铜的质量分数是多少?恰好完全反应时所得溶液的溶质质量分数是多少?(精确到0.1%)
抗癌新药紫杉醇的化学式为C 47H 51NO 14,回答下列问题:
(1)紫杉醇的相对分子质量为 ;
(2)紫杉醇中氮元素与氧元素的质量之比为 (写出最简整数比);
(3)13.86g紫杉醇中氢元素的质量为 g。
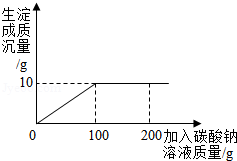
不纯的氯化钙样品中含有杂质氯化钠。取样品13.4g,全部溶于96.6g水中。向所得混合溶液中一定质量分数的碳酸钠溶液。如图所示曲线关系:
求:(1)恰好完全反应时,生成沉淀的质量是 g;
(2)恰好完全反应时,过滤,所得溶液中的溶质质量分数是多少?