(双选)某元素X的原子序数为52,下列叙述正确的是( )。
| A.X的主要化合价是-2、+4、+6 |
| B.X可以形成稳定的气态氢化物 |
| C.X的最高价氧化物对应水化物的酸性比HBrO4的酸性强 |
| D.X的简单阴离子的还原性比溴离子强 |
草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH)="=" 0时,c(H+,W)="=" 1 × 10-2 mol/L |
B.V(NaOH)< 10 mL时,不可能存在c(Na+)="=" 2 c(C2O )+ c(HC2O )+ c(HC2O ) ) |
| C.V(NaOH)="=" 10 mL时,c(H+,W)="=" 1 × 10-7mol/L |
D.V(NaOH)> 10 mL时,c(Na+)> c(C2O )>c(HC2O )>c(HC2O ) ) |
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1 mol N—N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则()
| A.N4的熔点比P4高 |
| B.1 mol N4气体转化为N2时要吸收724 kJ能量 |
| C.N4是N2的同系物 |
| D.1 mol N4气体转化为N2时要放出724 kJ能量 |
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+===Cu2++H2↑,则下列关于该装置的有关说法中正确的是()
| A.该装置可能是原电池,也可能是电解池 |
| B.该装置只能是原电池,且电解质溶液为硝酸 |
| C.该装置只能是电解池,且金属铜为该电解池的阳极 |
| D.该装置只能是原电池,电解质溶液不可能是盐酸 |
在N2(g)+3H2(g) 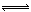 2NH3(g);△H<0。当分离出NH3后下列说法正确的是
2NH3(g);△H<0。当分离出NH3后下列说法正确的是
| A.平衡向逆向移动 | B.平衡不移动 |
| C.正反应速率先变大后变小 | D.逆反应速率先变小后变大 |
关于SiO2晶体的叙述中,正确的是( )
| A.通常状况下,60 g SiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数) |
| B.60 g SiO2晶体中,含有2NA个Si—O键 |
| C.晶体中与同一硅原子相连的4个氧原子处于同一四面体的4个顶点 |
| D.SiO2晶体中含有1个硅原子,2个氧原子 |