元素周期表在指导科学研究和生产实践方面具有十分重要的意义,请将下表中A、B两栏描述的内容对应起来。
| A |
B |
A |
B |
| ①制半导体的元素 |
(a)ⅢB至ⅥB的过渡元素 |
① |
|
| ②制催化剂的元素 |
(b)F、Cl、Br、N、S“三角地带” |
② |
|
| ③制耐高温材料的元素 |
(c)金属与非金属元素分界线附近 |
③ |
|
| ④制制冷剂的元素 |
(d)相对原子质量较小的元素 |
④ |
|
| ⑤地壳中含量较多的元素 |
(e)过渡元素 |
⑤ |
|
在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢(H2O2)为原料制取氧气,当制得同温、同压下相同体积的O2时,三个反应中转移的电子数之比为 ( )
| A.l :l :1 | B.2 :2 :l | C.2 :3 :1 | D.4 :3 :2 |
将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后所得的固体物质是
| A.Na2CO3、Na2SiO3 | B.Na2CO3、SiO2 | C.Na2SiO3 | D.SiO2 |
向50ml 1mol/L的KAl(SO4)2溶液中逐滴加入2mol/L的Ba(OH)2溶液,充分反应。下列说法正确的是
| A.当Al3+恰好完全沉淀时,消耗Ba(OH)2溶液30ml |
| B.当SO42—恰好完全沉淀时,Al3+全部转化为AlO2— |
| C.加入50mlBa(OH)2溶液时,反应可用下列离子方程式表示:2Al3++3SO42—+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓ |
| D.随加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大 |
NaCl是一种化工原料,可以制备一系列物质(见图)。下列说法正确的是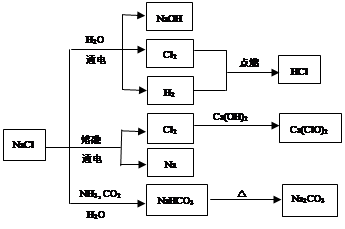
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.图中所示转化反应都是氧化还原反应 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
将Cu片放入0.1 mol·L-1 FeCl3溶液中,反应一定时间后取出Cu片,溶液中C(Fe3+):C(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为
| A.3:4 | B.3:5 |
| C.4:3 | D.3:2 |