有人设计以Pt和Zn为电极材料,埋入人体作某种心脏起搏器的能源。它依靠人体内体液中含有一定物质的量浓度的溶解氧、H+和Zn2+进行工作。试写出两极反应的方程式。
氮元素的单质及化合物在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式;
②NH3的稳定性比PH3(填写“强”或“弱”)。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。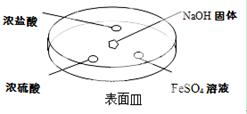
①浓盐酸液滴附近发生反应的化学方程式为。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是(写化学式,一种即可)。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2+ + 2NH3·H2O= Fe(OH)2↓+ 2NH4+ 和 _______。
(3)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式______________________________________;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明 。
(4)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。
已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3
写出氧化吸收法除去氮氧化物的化学方程式___________________。
(5)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为 _________ ,若反应中有3 mol电子发生转移时,生成亚硝酸的质量为g。
(共11分)(1)下列说法正确的是
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁的电化腐蚀中,吸氧腐蚀和析氢腐蚀的负极反应都为:Fe-2e- = Fe2+
C.可逆反应在一定条件下,有一定的限度,当反应进行到最大限度后,反应物就不再转化为生成物
D.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在 101 kPa 时,2g H2完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热化学方程式表示为;
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)  CH3OH(g) +H2O(g);
CH3OH(g) +H2O(g);
下图表示该反应进行过程中能量的变化。(单位为:kJ·mol-1)该反应是(填“吸热”或“放热”)反应。△H0(填“>”或“<”)。
(4)比较下面各组热化学方程式,△H1<△H2的是(即前一反应放热较多的是)。
A.2H2(g) + O2(g) = 2H2O(g ) △H12H2(g) + O2(g) = 2H2O(1) △H2
B.S(g) + O2(g) = SO2(g ) △H1 S(s) + O2(g) = SO2(g ) △H2
C.C(s) + 1/2O2(g) ="CO" (g ) △H1 C(s) +O2(g) =CO2 (g ) △H2
D.H2(g) + Cl2(g) ="2HCl(g" ) △H11/2H2(g) +1/2 Cl2(g) ="HCl(g" ) △H2
(5)101 kPa条件下,14g N2和3g H2反应生成NH3的能量变化如下图示意:
又已知:①已知b=1173;
②25 ℃、101 kPa下N2(g)+3H2 (g)  2 NH3 (g) △H =-92 kJ·mol-1
2 NH3 (g) △H =-92 kJ·mol-1
则a =。
据图回答下列问题: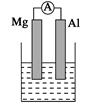
Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是___________________
负极反应式为:______________________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应化学方程式为____________________________________。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为______________。
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇(CH4OH)燃料电池的工作原理如下图所示。
①该电池工作时,b口通入的物质为_______,c口通入的物质为______。
②该电池正极的电极反应式为:_______
工业上用乙烯和氯气为原料合成聚氯乙烯(PVC)。已知次氯酸能跟乙烯发生加成反应,以乙烯为原料制取PVC等产品的转化关系如下图所示 。
。
试回答下列问题:
(1)写出有机物B和G的结构简式:B,G;
(2)写出D的所有可能的同分异构体的结构简式;
(3)写出④反应的化学方程式;
(4)写出⑥反应的化学方程式;
反应类型是;
(14分)已知实验室由 合成
合成 的反应流程如下(部分试剂和反应条件已略去) (X代表卤素原子,R代表烃基)
的反应流程如下(部分试剂和反应条件已略去) (X代表卤素原子,R代表烃基)
请回答下列问题:
(1)分别写出B、D的结构简式:B_______________、D_______________。
(2)反应①~⑦中属于消去反应的是____ (填数字代号)。属于加成反应的是________(填数字代号)。
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式还有:。
(4)试写出C→D反应的化学方程式(有机物写结构简式,并注明反应条件)。