KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去。某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响。该实验条件作如下限定:
①所用KMnO4酸性溶液的浓度可选择:0.02 mol·L-1、0.002 mol·L-1;
②所用H2C2O4溶液的浓度可选择:0.2 mol·L-1、0.4 mol·L-1;
③每次实验时KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液的用量均为2mL。
(1)若要探究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成____ 组实验进行对比即可得出结论。
(2)在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得实验数据(从混合振荡均匀开始计时)如下表所示:
| KMnO4酸性溶液浓度 (mol·L-1) |
溶液褪色所需时间(min) |
|
||
| 第一次 |
第二次 |
第三次 |
||
| 0.02 |
14 |
13 |
11 |
|
| 0.002 |
6.7 |
6.6 |
6.7 |
|
①用0.002 mol/L KMnO4酸性溶液进行实验时,KMnO4的平均反应速率(忽略混合前后溶液体积变化)。
②依据表中数据,不能得出“溶液的褪色所需时间越短,反应速率越快”的结论。某同学设计以下方案,可以直接得出“褪色时间越短,反应的速率越快”结论。
| KMnO4酸性溶液 |
H2C2O4溶液 |
||
| 浓度/ mol/L |
体积(ml) |
浓度/ mol/L |
体积(ml) |
| 0.02 |
2 |
b |
4 |
| a |
2 |
c |
4 |
则表中a= ;b= ;c= 。
(3)草酸电离常数:Ka1=5.9×10-2,Ka2=6.4×10-5。与KMnO4反应时,它将转化为CO2和H2O。
①草酸与酸性高锰酸钾溶液反应的离子方程式为 。
②室温下,0.1mol·L-1 KHC2O4酸溶液中pH 7,理由是 。
(4)测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图。请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因: 。
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成。乙醇和汽油经加工处理形成的车用燃料即乙醇汽油。结合有关知识,回答下列问题:
(1)在试管里加入2mL乙醇。把一端弯成螺旋状的铜丝放在酒精外焰中加热,使铜丝表面生成一薄层黑色的氧化铜,立即把它插入盛有乙醇的试管里(如图),取出铜丝,可以观察到铜丝表面。
(2)写出乙醇与氧气催化氧化的化学反应方程式。
(3)乙醇汽油作为一种新型车用燃料,符合我国的能源战略,推广使用乙醇汽油的好处是(写出一条即可)。
(3分)已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。
请回答下列问题:
(1)维生素A1是一类重要的维生素,写出其含氧官能团的名称。
(2)维生素A1的结构简式如上图,若1mol维生素A1分子最多可跟__ molH2发生加成反应
(8分)(1)A、B两元素均位于周期表中第三周期,它们的原子核外最外层电子数之和为7,其中A元素的原子核外最外层电子数为1个,两者间可形成化合物A2B。根据以上条件回答:
①写出A、B的元素符号:A,B
②写出化合物A2B的电子式。
(2) 现有A、B、C、D四种物质,它们之间能发生如下图所示的转化关系
溶液B、C中都含有金属元素E,溶液B的颜色为黄色。请根据以上信息回答下列问题:
①写出金属E元素符号:
②写出金属A和溶液B反应的离子方程式:
③为了检验溶液B中金属阳离子,通常加入的试剂是
(4分)(1) 写出乙醇与乙酸反应生成酯的化学方程式。
(2) 写浓盐酸与二氧化锰加热反应来制取氯气的化学方程式_________。
如右图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色。当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol·L-1。经过 60s,乙容器中的反应达到平衡。(反应过程中两个容器的温度均保持恒定)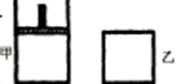
(1)容器中气体出现红棕色的原因(用化学方程式表示)是:。(2)前 2s内乙容器中以N2O4的浓度变化表示的反应速率为。
(3)达到平衡时,甲容器中反应所需的时间60s(填“大于”、“小于”或“等于”,以下同);容器内N2O4的浓度甲乙;反应过程中吸收的能量甲乙。