双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如图所示。
(1)双酚A中的含氧官能团为 (填名称)。
(2)下列关于双酚A的叙述中,不正确的是 (填标号)。
A.遇FeCl3溶液变色
B.可以发生还原反应
C.1 mol双酚A最多可与2 mol Br2反应
D.可与NaOH溶液反应
(3)双酚A的一种合成路线如下图所示:
①丙烯→A的反应类型是 。
②B→C的化学方程式是 。
Ⅱ甲苯和溴乙烷混合物可通过如下流程进行分离。 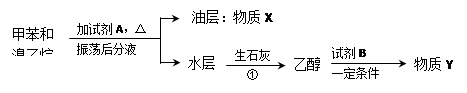
请填写下列空白:
(1)X的结构简式为 ;
(2)操作①能否用分液 ,理由是 。
(3)写出甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式: 。
(4)如果Y为乙烯,则试剂B为 ,“一定条件”是指 。
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为________。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是________(填序号)。
a.Cl2、Br2、I2的熔点b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
①完成Ⅰ中反应的总化学方程式:
②Ⅱ中转化的基本反应类型是________________,该反应过程能析出KClO3晶体而无其他晶体析出的原因是____________________________________。
(4)一定条件下,在水溶液中1 mol Cl-、ClO(x=1,2,3,4)的能量(kJ)相对大小如右图所示。
①D是________(填离子符号)。
②B→A+C反应的热化学方程式为________________(用离子符号表示)。
(10分)某种溶液仅含下表离子中的5种(不考虑水的电离与离子水解),且各种离子的物质的量均为1 mol。
| 阳离子 |
K+ Ba2+ Fe2+ Al3+ Fe3+ Mg2+ |
| 阴离子 |
OH- HCO3- CO32- Cl- NO3- SO42- |
若向原溶液中加入足量的盐酸,有无色气体生成。经分析反应后溶液中阴离子的种类没有变化。
(1)溶液中______(填“一定”、“一定不”或“可能”)含有HCO3-或CO32-,理由是________________。
(2)原溶液中所含的阴离子为__________,阳离子为__________。
(3)向原溶液中加入足量的盐酸,有无色气体生成的离子反应方程式为__________________。
(4)若向原溶液中加入足量的氢氧化钠溶液,充分反应后将沉淀过滤、洗涤、干燥灼烧至恒重,得到固体质量为__________g。
(一)下列各组离子在指定溶液中一定能大量共存的是___________________。
①无色溶液中:K+、Na+、MnO 、SO
、SO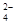
②甲基橙呈黄色的溶液中:I-、Cl-、NO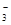 、Na+
、Na+
③石蕊呈蓝色的溶液中:Na+、AlO 、NO
、NO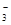 、HCO
、HCO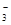
④在pH=1的溶液中:Fe2+、NO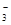 、SO
、SO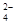 、Na+
、Na+
⑤在pH=0的溶液中:Na+、NO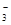 、SO
、SO 、K+
、K+
⑥在pH=12的溶液中:K+、Cl-、HCO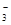 、Na+
、Na+
⑦含大量OH-的溶液中:CO 、Cl-、F-、K+
、Cl-、F-、K+
⑧ =1012的溶液中:NH
=1012的溶液中:NH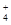 、Al3+、NO
、Al3+、NO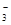 、Cl-
、Cl-
⑨加入Al能放出H2的溶液中:Cl-、HCO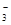 、SO
、SO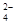 、NH
、NH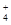
⑩由水电离出的c(OH-)=10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO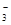
⑪c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO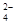 、SCN-
、SCN-
⑫含大量Al3+的溶液中:K+、Na+、NO 、ClO-
、ClO-
(二)三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为____________。
(2)写出该反应的化学方程式_____________________________________。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现.你判断该气体泄漏时的现象是_______________________________________。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有______________________________(填化学式)。
(每空2分,作图3分,共13分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是Al3+和________,阴离子是________。
(2)试通过计算确定:n(Al3+)=________;该结晶水合物的化学式________。
(3)假设过程中向该溶液中加入的Ba(OH)2溶液的物质的量浓度为2.0mol/L。
①加入mLBa(OH)2溶液时,所得沉淀的总物质的量最大。
②请在下图中画出生成沉淀的物质的量与加入Ba(OH)2溶液体积的关系示意图。
(每空2分,共12分)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是(写化学式)。
(2)写出并配平该反应的化学方程式:
(3)发生氧化反应的物质是,反应中4mol的氧化剂能(填“失去”或
“得到”)mol电子.
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为。