X、Y、Z、W、R属于短周期元素。已知它们都不是稀有气体元素,X的原子半径最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2∶1。下列叙述错误的是( )
| A.X与Y形成的两种化合物中阴、阳离子的个数比均为1∶2 |
| B.Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物低 |
| C.Z、W、R最高价氧化物对应水化物的酸性强弱顺序:R>W>Z |
| D.Y分别与Z、W、R以两种元素组成的常见化合物有5种 |
已知25 ℃时,BaCO3的溶度积Ksp=2.58×10-9,BaSO4的溶度积Ksp=1.07×10-10,则下列说法不正确的是
| A.温度一定时,当溶液中c(Ba2+)×c(SO42-)=1.07×10-10时,此溶液为BaSO4的饱和溶液 |
| B.因为Ksp(BaCO3)>Ksp(BaSO4),所以无法将BaSO4转化为BaCO3 |
| C.25 ℃时,在未溶解完BaCO3的饱和溶液中滴入少量Na2SO4溶液后有BaSO4沉淀析出,此时溶液中c(CO32-)∶c(SO42-)=24.11 |
| D.在饱和BaCO3溶液中加入少量Na2CO3固体,可使c(Ba2+)减小,BaCO3的溶度积不变 |
下列溶液中有关微粒的物质的量浓度关系正确的是
| A.常温下,将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合溶液中:c(Na+)=c(CH3COO-) |
| B.相同条件下pH=5的①NH4Cl溶液 ②CH3COOH溶液 ③稀盐酸溶液中由水电离的c(H+):①>②>③ |
| C.pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中,c(NH4+)大小顺序:①=②>③ |
| D.0.1mol/L醋酸钡溶液中,c (Ba2+)>c(CH3COO-)>c(OH-)> c (H+) |
下列操作或仪器的选用正确的是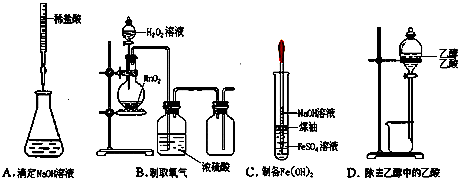
下列表述正确的是
A.比例模型为: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 |
B.2CH3CH2OD+O2 2CH3CHO+2DHO 2CH3CHO+2DHO |
| C.二氧化硫、氨、煤的液化均为物理变化 |
D.实验室中制取乙酸乙酯的方程式为:CH3COOH+H18O-C2H5 CH3COOC2H5+H218O CH3COOC2H5+H218O |
下列关于有机物的说法中不正确的是
| A.乙烯、苯、乙酸分子中的所有原子都在同一平面上 |
| B.正丁烷和异丁烷的熔、沸点不相同 |
| C.C4H9Br的同分异构体有4种 |
| D.乙烯和甲烷可用酸性高锰酸钾溶液鉴别 |