下列物质转化在给定条件下能实现的是( )
①Al2O3NaOH(aq),NaAlO2(aq) Al(OH)3
Al(OH)3
②S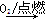 SO3
SO3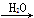 H2SO4
H2SO4
③饱和NaCl(aq)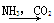 NaHCO3
NaHCO3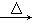 Na2CO3
Na2CO3
④Fe2O3 FeCl3(aq)
FeCl3(aq)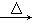 无水FeCl3
无水FeCl3
⑤MgCl2(aq) Mg(OH)2
Mg(OH)2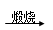 MgO
MgO
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
下列说法正确的是
| A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有还原性 |
| B.粗锌与稀硫酸反应比纯锌快,说明粗锌反应时形成了原电池 |
| C.硬水含有Ca2+、Mg2+、HCO3-、SO42-,煮沸可以完全除去其中的Ca2+、Mg2+ |
| D.pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强 |
下列实验的解释或结论不正确的是
| 选项 |
实验 |
解释或结论 |
| A |
用激光笔照射水玻璃溶液,有丁达尔现象 |
SiO32-水解生成硅酸胶体 |
| B |
在新制的氯水中加入碳酸钙粉末,充分搅拌 |
氯水中HClO的物质的量增加 |
| C |
向包有Na2O2的脱脂棉滴少量水,脱脂棉燃烧 |
Na2O2与H2O反应放热并有O2生成 |
| D |
向某溶液中加入稀盐酸,再加入硝酸钡溶液生 成白色沉淀 |
原溶液中一定存在SO42- |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.含有NA个NO2、N2O4分子的混合气体降低温度,混合气体的分子数目小于NA |
| B.常温常压和光照条件下,33.6 LCl2与3.0g H2反应,生成的HCl分子数目为3NA |
| C.1.68 g Fe和足量水蒸气反应,转移的电子数目为0.09NA |
| D.一定条件下,1 mol N2和3 mol H2充分反应,生成物中含N—H键数目为6NA |
下列实验装置及操作正确的是
| A.制备乙酸乙酯 | B.构成原电池 | C.检验有无乙烯生成 | D.检查装置气密性 |
下列离子方程式书写正确的是
| A.AgCl沉淀在氨水中溶解:AgCl+2NH3·H2O ==Ag(NH3)2++Cl—+2H2O |
| B.向Na2SO3、NaI的混合溶液中滴加少量氯水:2I—+C12="=2" Cl—+I2 |
C.向水杨酸中加入适量Na2CO3溶液: |
D.用铜片作阴、阳极电解硝酸银溶液:4Ag +2H2O +2H2O 4Ag+O2↑+4H 4Ag+O2↑+4H |