纳米是长度单位,1纳米等于1×10-9 m,物质的颗粒达到纳米级时,具有特殊的性质。例如将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧。下列对“纳米铜”的有关叙述正确的是( )
| A.常温下“纳米铜”比铜片的金属性强,反应时反应速率快 |
| B.常温下“纳米铜”比铜片更易失电子,反应时反应速率快 |
| C.常温下“纳米铜”的还原性大于铜片的还原性 |
| D.“纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快 |
在电冶铝的电解槽中存在电解质W3XZ6—XZ3—X2Y3,己知X、Y、Z、W四种元素的简单离子的电子层结构均相同。X原子最外层电子数等于电子层数,则下列说法正确的是
| A.原予序数:W>X>Y>Z |
| B.原子半径:r(W)>r(X)>r(Y)>r(Z) |
| C.最高价氧化物对应的水化物碱性:W<X |
| D.在电解过程中,W3XZ6的主要作用是增强电解质的导电性 |
25℃时,向20.00 mL的NaOH溶液中逐滴加入某浓度的CH3COOH溶液。滴定过程中,溶液的pH与滴入CH3COOH溶液的体积关系如图所示,点②时NaOH溶液恰好被中和。则下列说法中,错误的是
| A.CH3COOH溶液的浓度为0.1 mol·L-1 |
| B.图中点①到点③所示溶液中,水的电离程度先增大后减小 |
| C.点④所示溶液中存在:(CH3COOH)+c(H+)=c(CH3COO-)+c(OH-) |
| D.滴定过程中会存在:c(Na+)> c(CH3COO-)=c(OH-)> c(H+) |
下列叙述正确的是
| A.标准状况下,2.24 L C12溶于水,转移6.02×1022个电子 |
| B.Na2S在空气中长期放置变浑浊的离子方程式为:2S2-+O2+4H+=2S+2H2O |
| C.NaHCO3溶液中滴加少量NaOH溶液的离子方程式为:HCO3-+OH-=CO32-+H2O |
| D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3-能够大量共存 |
下述实验方案能达到实验目的的是
某有机物M的结构简式如图所示,下列叙述正确的是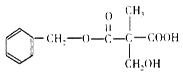
| A.其分子式为C12H12O5 |
| B.M中含有2种含氧官能团 |
| C.M能够发生加成、取代和加聚反应 |
| D.1 mol M和足量的NaOH溶液反应,可以消耗2 mol NaOH |