下列电离方程式正确的是( )
A.NaHSO4 Na++HSO4— Na++HSO4— |
B.NaHCO3 Na++H++CO3— Na++H++CO3— |
C.H3PO4 3H++PO43— 3H++PO43— |
D.HF H++F- H++F- |
有机物(如图)是甲烷被苯基取代的产物,下列说法不正确的是
| A.分子式为C25H20 |
| B.所有碳原子在一个平面上 |
| C.此物质属于芳香烃 |
| D.此物质不属于苯的同系物 |
既能使溴水和酸性高锰酸钾溶液褪色,又能跟银氨溶液溶液反应的物质是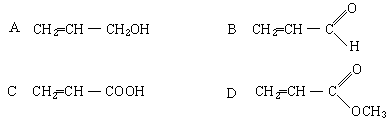
下列关于同系物的说法错误的是
| A.同系物能符合同一通式 |
| B.同系物具有相同的最简式 |
| C.相邻的同系物在组成上相差一个CH2原子团 |
| D.同系物的化学性质基本相似,物理性质随着碳原子数增加而有规律的变化 |
从溴水中萃取溴,下列试剂中能用做萃取剂的是
| A.乙酸 | B.水 | C.四氯化碳 | D.酒精 |
在实验室中通常以加热乙醇和浓硫酸的混合液来制取乙烯,在这个反应里浓硫酸
| A.既是反应物又是脱水剂 | B.既是反应物又是催化剂 |
| C.既是催化剂又是脱水剂 | D.仅是催化剂 |