向存在大量K+、Cl-的溶液中通入足量CO2后,该溶液中还可能大量存在的离子组是( )
| A.Na+、Br-、CO32- | B.AlO2-、Na+、MnO4- |
| C.NH4+、Na+、SO42- | D.Na+、Ag+、NO3- |
下列变化过程中,熵在减小(即△S<O)的是( )
A.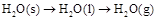 |
B.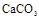 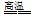 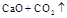 |
C.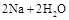 ══ ══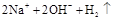 |
D.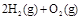 ══ ══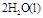 |
常温下,浓度均为0.1mol·L-1的六种溶液的pH如下表:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
Na2SO4 |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是 .
②根据表中数据,浓度均为0.01mol·L-1的下列五种物质的溶液中,酸性最强的
是 (填字母);将各溶液分别稀释100倍,pH变化最小的是 (填字母).
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
铁和氧化铁的混合物共a mol,加 盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为()
盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为()
A.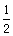 (a+b) mol (a+b) mol |
B.(a-b) mol | C.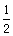 (a-b)mol (a-b)mol |
D.(a+b) mol |
下列表述中正确的是()
| A.任何能使熵值减小的过程都能自发进行 |
B.已知:2SO2(g)+O2(g) 2SO3(g):△H=-197kJ/mol.实验测得4molSO2参加上述反应放出354kJ热量,则SO2的转化率最接近于90% 2SO3(g):△H=-197kJ/mol.实验测得4molSO2参加上述反应放出354kJ热量,则SO2的转化率最接近于90% |
| C.在Na2SO4溶液中加入过量的BaCl2后,溶液中不存在SO42- |
| D.1mol NaOH分别和1mol CH3COOH、1molHNO3反应,后者比前者△H大 |
对下列各溶液中,微粒的物质的量浓度关系表述正确的是
| A.某溶液中存在的离子只有Cl-、OH-、NH4+、H+,该溶液中离子浓度大小关系可能为c(Cl-)>c(NH4+) >c(OH-)>c(H+)() |
| B.在NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) |
| C.将相同物质的量浓度的某弱酸(A-为弱酸根)溶液与KA溶液等体积混匀,测得混合后溶液pH=10,则混合液中c(K+)>c(A-) |
| D.0.1 mol·L-1 CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |