下列叙述正确的是( )
| A.含1 mol H2SO4的浓硫酸中有n(H+)=2n(SO42-)=2 mol |
| B.含1 mol H2SO4的浓硫酸和足量的锌完全反应,转移的电子为2 mol |
| C.配制2.0 mol·L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确) |
| D.用铜电极电解2.0 mol·L-1的硫酸,阴阳两极生成气体的体积之比为2∶1 |
密度为ρ g·cm-3的溶液b mL,含有相对分子质量为Mr的溶质a g,其物质的量浓度为cb mol·L-1,质量分数为W。则下列关系式不正确的是( )
A.cB= mol·L-1 mol·L-1 |
B.a="ρ·b·w" g |
C.ρ=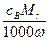 g·cm-3 g·cm-3 |
D.w=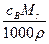 % % |
20 ℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是()
| A.25 ℃时,饱和KCl溶液的浓度大于4.0 mol·L-1 |
B.此溶液中KCl的质量分数为 ×100% ×100% |
| C.20 ℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液 |
| D.将此溶液蒸发部分水,再恢复到20 ℃时,溶液密度一定大于1.174 g·cm-3 |
实验室常用98%(密度为1.84 g·mL-1)的浓硫酸配制1∶4的稀硫酸,此稀硫酸的密度为1.23 g·mL-1,则其物质的量浓度为( )
| A.4.6 mol·L-1 | B.5.7 mol·L-1 |
| C.3.88 mol·L-1 | D.18.4 mol·L-1 |
体积相同的某营养液两份,其配方如下:
| KCl |
K2SO4 |
ZnSO4 |
ZnCl2 |
|
| (1) |
0.3 mol |
0.2 mol |
0.1 mol |
— |
| (2) |
0.1 mol |
0.3 mol |
— |
0.1 mol |
两份营养液中各离子浓度()
| A.完全相同 | B.完全不同 |
| C.仅c(K+)相同 | D.仅c(Cl-)相同 |
在标准状况下,某气体在水中溶解度为A,已知该物质的相对分子质量为Mr,那么此时1 L水中最多溶解此种气体的质量是( )
| A.22.4·A·Mrg | B.1 000·A·Mrg |
C.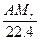 g g |
D.10·A g |