中学化学实验中,淡黄色的pH试纸常用于测定溶液的酸碱性。在25 ℃时,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在平衡:H2O H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是 (填字母)。
H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是 (填字母)。
| A.向水中加入NaHSO4 |
| B.向水中加入Cu(NO3)2 |
| C.加热水至100 ℃[其中c(H+)=1×10-6 mol·L-1] |
| D.在水中加入(NH4)2SO4 |
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显 色,溶液呈 性(填“酸”、“碱”或“中”);若用pH计测定,则pH 7(填“>”、“<”或“=”),溶液呈 性(填“酸”、“碱”或“中”)。
(10分) 氨气是一种重要的化工原料,工业上用N2和H2合成NH3。现已知N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化示意图如下左图。回答下列问题:
(1)该反应为(填“吸热”或“放热”)反应。
(2)合成氨的热化学方程式为。
(3)若又已知键能数据如上表,结合以上数据求出N-H键键能为kJ/mol。
(4)工业上,以氨气为原料生产硝酸的第一步为氨催化氧化,请写出该反应的化学方程式。
(10分)(I) 海带中含有碘元素,某校研究性学习小组设计了如下实验步骤来提取碘:
①在滤液中,滴加几滴硫酸和适量的双氧水②将海带烧成灰,向灰中加水,加热搅拌
③加CC14振荡、静置④过滤⑤分液。
(1)合理的操作顺序为。
(2)步骤③中要用到的玻璃仪器为,该步分离I2的操作叫。
(II)向某含有Fe2+、I—、Br—的溶液中缓缓通入适量氯气,溶液中各种离子的物质的量变化如图所示。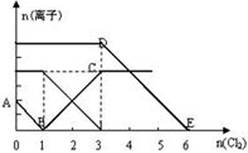
(3)AB段表示离子的减少。
(4)n(Cl2)=2mol时,溶液中反应的离子方程式为。
(17分)Na2SO3固体在空气中久置容易变质 。
(I)Na2SO3固体在空气中变质的主要原因,用化学方程式表示为。
(II)为探究Na2SO3样品的变质情况,现提出以下假设:
假设1:Na2SO3样品完全变质; 假设2:Na2SO3样品完全没有变质;假设3:。
补充完成以下实验过程及现象和结论,完成探究。
| 实验操作 |
现象和结论 |
| 步骤1:取少许样品于试管中,加入适量蒸馏水充分溶解,再滴加H2SO4酸化的KMnO4溶液; |
现象:若KMnO4溶液的紫红色褪为无色 ①结论:样品中有离子,假设1不成立。 ②褪色的离子方程式为: 。 |
| 步骤2:另取少许样品于试管中,加入适量蒸馏水充分溶解,再滴加稀HCl,使溶液呈酸性,再滴加适量BaCl2溶液; |
③现象:若 ; 结论:假设2成立。 |
| …… |
…… |
(III)为测定某无水Na2SO3固体样品的纯度,甲同学设计了下图实验。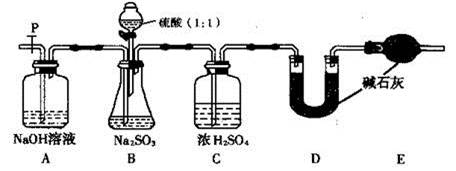
检查B装置气密性的操作为。
(2)实验中待锥形瓶中不再产生气体后,打开活塞P从导管左端缓缓鼓入一定量的空气,这样做的目的是。
(3)除已称量的a g Na2SO3样品外,实验中还应测定的数据是处(填图中字母)装置实验前后的质量差。
(14分)有A、B、C、D、F、G六种短周期主族元素,它们的原子序数依次增大。B元素的最高正价与最低负价的绝对值相等,D元素原子最外层电子数是次外层电子数的3倍,F元素在地壳中含量居第二位;A与B、C、D分别构成电子数相等的分子Q、X、Y;化合物AG在空气中与X反应产生白烟Z。
请回答下列问题:
G的原子结构示意图为,A2D2电子式为,
BD2的结构式为,Q的分子空间结构为。
(2)固体Z为晶体(填晶体类型),Z中所含化学键类型有。
(3)在D同主族元素氢化物中,Y的沸点反常,原因是。
(4)B、F、G元素非金属性由强到弱的顺序为,若用下图装置验证这三种元素非金属性强弱,则在装置中加入的试剂分别为:Ⅰ,Ⅱ,Ⅲ。(填化学式)
下图是研究铜与浓硫酸的反应装置: 
(1)A试管中发生反应的化学方程式为。
(2)反应一段时间后,可观察到B试管中的现象为。
(3)C试管口浸有NaOH溶液的棉团作用是。
(4)实验结束后,证明A试管中反应所得产物是否含有铜离子的操作方法是。
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
| 资料1 |
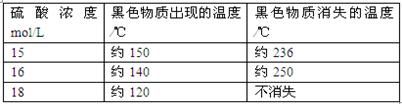 附表铜与浓硫酸反应产生黑色物质的相关性质 |
| 资料2 |
X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。 |
仅由上述资料可得出的正确结论是。
A.铜与浓硫酸反应时所涉及的反应可能不止一个 B.硫酸浓度选择适当,可避免最后产物中出现黑色物质;C.该反应发生的条件之一是硫酸浓度≥15 mol·L D.硫酸浓度越大,黑色物质越快出现、越难消失