美国化学家R.F.Heck因发现Heck反应而获得2010年诺贝尔化学奖。例如经由Heck反应合成一种防晒剂:
反应①: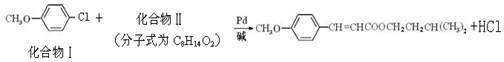
化合物Ⅱ可由以下合成路线获得:
(1)化合物I核磁共振氢谱显示存在 组峰,化合物I的分子式为 。
(2)1mol化合物Ⅱ完全燃烧最少需要消耗 mol O2,其完全水解的化学方程式为 (注明条件)。
(3)化合物Ⅲ中含氧官能团的名称是 ;化合物Ⅴ与浓H2SO4共热生成化合物Ⅵ,化合物Ⅵ能使酸性KMnO4溶液褪色,化合物Ⅵ的结构简式是 。
(4)化合物Ⅰ的一种同分异构体化合物Ⅶ符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色。化合物Ⅶ与过量NaOH溶液共热,发生反应的方程式为 。
(1)在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇立即变色的是,常用于自来水杀菌、消毒的是,能用向下排空气法收集的是,溶于水后能生成强酸的是。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒消毒剂。
①工业上通过下列方法制取ClO2,完成该反应的化学方程式:2KClO3 + SO2 =2C1O2+
②配平下列化学方程式:KClO3+H2C2O4+H2SO4=ClO2↑+K2SO4+CO2↑+H2O
下列有关上述反应的说法正确的是。
| A.H2C2O4在反应中被还原 | B.KClO3是氧化剂 |
| C.ClO2是还原剂 | D.生成1molClO2有2mol电子转移 |
(6分)某固体混合物可能由KCl、Na2SO4、KI、CuCl2、CaCl2和Na2CO3中的一种或几种组成。依次进行下列实验:
①混合物加水得无色透明溶液;
②向上述溶液中加入过量BaCl2溶液有白色沉淀生成,将沉淀滤出;
③上述白色沉淀可部分溶于稀盐酸;
④往上述滤液中加入AgNO3溶液,有白色沉淀生成,再加稀硝酸沉淀不溶解。根据以上实验推断:混合物中肯定含有;
肯定没有;
可能含有。
实验室需配制500mL 0.2mol/L NaCl溶液
(1)本实验用到的仪器已有药匙、烧杯、量筒、托盘天平(砝码、镊子)、玻璃棒、胶头滴管,还缺少的玻璃仪器是。
(2)配制时,需称取NaCl的质量是g。
(3)在配制过程中,其他操作都正确的情况下,下列操作会导致所配制的溶液浓度偏高的是。(选填序号)
①引流后没有洗涤烧杯和玻璃棒
②加蒸馏水时,不慎超过了刻度,取出少量水使液面恰好到刻度线
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视标线
⑤定容时仰视标线
将燃着的木条伸入充满CO2的集气瓶中,观察到的现象是;将燃着的镁条伸入充满CO2的集气瓶中,观察到的现象是,
反应的化学方程式为。
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为:。
(2)漂白粉的有效成分是。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为。