电化学在日常生活中用途广泛,图甲是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2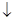 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2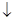 |
| B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| C.图乙电解池中,若有0.084 g阳极材料参与反应,则阴极会有336 mL的气体产生 |
| D.若图甲燃料电池消耗3.6 g镁产生的电量用以图乙废水处理,理论上可产生10.7 g氢氧化铁沉淀 |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是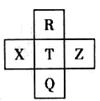
| A.非金属性:Z<T<X |
| B.最高价氧化物的水化物的酸性:Q>T |
| C.气态氢化物稳定性:R<T<Q |
| D.R与Q的电子数相差26 |
“封管实验”具有简易、方便、节约、绿色等优点,观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是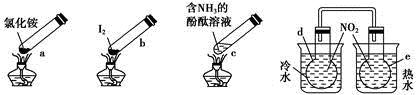
| A.加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 |
| C.加热时,c中溶液红色变深,冷却后又变浅 |
| D.e内气体颜色变浅,d内气体颜色加深 |
下列现象或事实可用同一原理解释的是
| A.浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| B.铁在冷的浓硫酸中和铝在冷的浓硝酸中都没有明显变化 |
| C.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色 |
| D.漂白粉和水玻璃长期暴露在空气中变质 |
下列物质间的转化在给定条件下能一步实现的是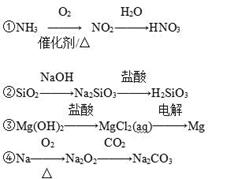
| A.①②③ | B.③④ | C.①④ | D.②④ |
X、Y、P、Q四种短周期元素,元素X在地壳中含量最高,充有元素Y单质蒸气的灯透雾能力强,常用于道路和广场的照明,Q的最外层电子数与其电子总数比为3:8,P的单质常用作电脑的芯片材料。
| A.元素Y、P的简单氢化物中化学键类型相同 |
| B.原子半径:X>Y |
| C.最高价氧化物的水化物酸性:P<Q |
| D.X、Q两元素的最高正化合价相同 |