共聚法可改进有机高分子化合物的性质,高分子聚合物P的合成路线如下: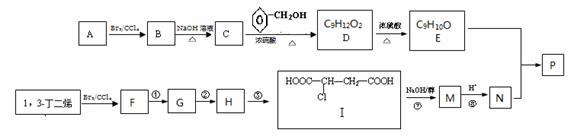
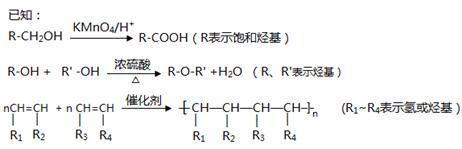
(1)A的结构式为________________ ,C的名称为
(2)D中含有的官能团的名称
(3)由F经①~③合成I,F可以使溴水褪色.反应①的化学方程式是 。
反应②的反应类型是 反应③的反应试剂是 。
(4)下列说法正确的是 。
a.C可与水任意比例混合
b.A与1,3-丁二烯互为同系物
c.由I生成M时,1mol I最多消耗3molNaOH
d.N不存在顺反异构体
(5)写出由D生成E的化学方程式 。
(6)E与N等物质的量发生共聚反应生成P,则P的结构简式为 。
(7)E有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式 。
a.苯环上有两个取代基
b.能使FeCl3液显紫色
c.1mol该有机物与浓溴水反应时能消耗4molBr2
口服抗菌药利君沙的制备原料G和某种广泛应用于电子电器等领域的高分子化合物Ⅰ的合成路线如下:
已知:①R—CH2—CH===CH2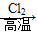 R—CHCl—CH===CH2
R—CHCl—CH===CH2
②R—CH2—CH===CH2 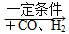 R—CH2CH2CH2CHO
R—CH2CH2CH2CHO
(1)A的结构简式是________,D中的官能团的名称是________。
(2)写出B―→C的化学方程式:___________________________________________,
该反应类型是____________________。
(3)H的分子式为C8H6O4,能与碳酸钠溶液反应放出气体,其一氯取代物只有一种,写出H的结构简式:_____________________________________________________
(4)写出E+H―→I的化学方程式:______________________________。
(5)J是比C多一个碳原子的C的同系物,J可能的稳定结构有________种(①考虑顺反异构;②“ ”结构不稳定),请任意写出其中一种的结构简式:______________。
”结构不稳定),请任意写出其中一种的结构简式:______________。
(6)关于G的说法中正确的是________(填序号)。
a.1 mol G可与2 mol NaHCO3反应
b.G可发生消去反应
c.1 mol G可与2 mol H2发生加成反应
d.G在一定条件下可与Cl2发生取代反应
可降解聚合物P的合成路线如下: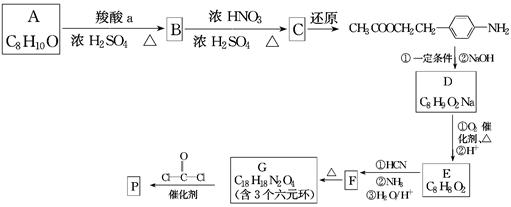
已知:
(R为烃基)
(1)A的含氧官能团名称是________。
(2)羧酸a的电离方程式是_______________________________________________。
(3)B→C的化学方程式是_________________________________________________。
(4)化合物D苯环上的一氯代物有2种,D的结构简式是_______________________。
(5)E→F中反应①和②的反应类型分别是________。
(6)F的结构简式是_____________________________________________________。
(7)聚合物P的结构简式是_______________________________________________。
生活中常用的某种香料X的结构简式为
(1)香料X中含氧官能团的名称是________。
(2)香料X可发生的反应类型是________(填代号)。
a.酯化反应 b.还原反应 c.加成反应 d.消去反应
(3)已知: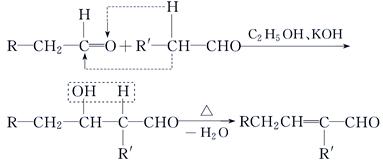
香料X的合成路线如下: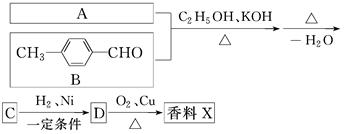
①A的结构简式是________。
②检验有机物C中含有碳碳双键所需用的试剂是________。
a.银氨溶液 b.酸性高锰酸钾溶液 c.溴水 d.氢氧化钠溶液
③D→X的化学方程式为___________________________________________。
④有机物B的某种同分异构体E具有如下性质:
a.与浓溴水反应生成白色沉淀,且1 mol E最多能与4 mol Br2反应
b.红外光谱显示该有机物中存在碳碳双键则E的结构简式为________。
已知: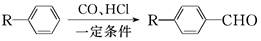
为合成某种液晶材料的中间体M,有人提出如下不同的合成途径: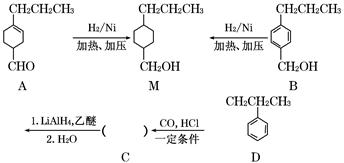
(1)常温下,下列物质能与A发生反应的有________(填序号)。
a.苯 b.Br2/CCl4 c.乙酸乙酯 d.KMnO4/H+溶液
(2)M中官能团的名称是________,由C→B的反应类型为________。
(3)由A催化加氢生成M的过程中,可能有中间生成物 和________(写结构简式)生成
和________(写结构简式)生成
(4)检验B中是否含有C可选用的试剂是________(任写一种名称)。
(5)物质B也可由C10H13Cl与NaOH水溶液共热生成,C10H13Cl的结构简式为________。
(6)C的一种同分异构体E具有如下特点:
a.分子中含—OCH2CH3
b.苯环上只有两种化学环境不同的氢原子
写出E在一定条件下发生加聚反应的化学方程式:____________________________。
化合物A(C12H16O2)经碱性水解、酸化后得到B和C(C8H8O2)。C中含有苯环,且苯环上有2种氢原子。B经过下列反应后得到G,G由碳、氢、氧三种元素组成,相对分子质量为172,元素分析表明,含碳55.8%,含氢7.0 %,核磁共振氢谱显示只有一个峰。
请回答下列问题:
(1)A的结构简式为_______________,G的分子式为______________。
(2)B的名称为_____________,D中官能团的名称为________________。
(3)写出F→G的化学方程式:________________________________,该反应属于_________(填反应类型)。
(4)写出满足下列条件的C的3种同分异构体的结构简式:___________________。
①是苯的对位二取代化合物;②能与FeCl3溶液发生显色反应;③不考虑烯醇( )结构。
)结构。
(5)在G的粗产物中,经检测含有聚合物杂质。写出聚合物杂质可能的结构简式(写出1种即可):_________________________________________________________________。