X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X是元素周期表中原子半径最小的元素,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。 请回答下列问题:
(1)Y在元素周期表中的位置为 ,ZX的电子式为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作消毒剂的有 、 (写出其中两种物质的化学式)。
(4)X2M的标准燃烧热ΔH=-a kJ·mol-1,写出表示X2M标准燃烧热的热化学方程式: 。
下表是元素周期表的短周期部分,表中字母分别表示一种元素。
请回答下列问题:
(1)g与b可形成离子化合物b2g2,该物质含有的化学键类型有 ________。
(2)e、f、g三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示)________。
(3)从化合物c2g3与eg2组成的混合物中分离提纯eg2,可加入上述________(用元素符号表示)两种元素形成化合物的水溶液后再过滤洗涤。
(4)a、d两种元素可形成多种化合物,其中化合物X的产量是衡量一个国家石油化工发展水平的标志。X可与H2O在一定条件下反应生成化合物A,该反应的化学方程式为:________________________。
(5)航天技术中常使用a和g单质组成的燃料电池,该电池具有高能、轻便和不污染环境等优点。该电池反应为____________________。
分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题: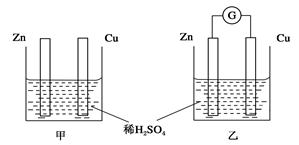
(1)以下叙述中,正确的是__________。
| A.甲中锌片是负极,乙中铜片是正极 |
| B.两烧杯中铜片表面均有气泡产生 |
| C.两烧杯中溶液pH均增大 |
| D.产生气泡的速度甲中比乙中慢 |
E.乙的外电路中电流方向Zn→Cu
(2)变化过程中能量转化的形式主要是:甲为__________;乙为__________。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是__________。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式_________________
已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出元素符号:
A:, B:,C:_______,D:____。
(2)画出E的阴离子的结构示意图:。
(3)C的单质和D的单质在一定条件下反应生成化合物X,该反应的化学方程式为。
(4)A分别与其他四种元素形成的化合物,水溶液显碱性的是(写化学式)。
(5)将12 g B单质在足量的D单质中燃烧,所得气体通入1 L 1 mol·L-1NaOH溶液中发生反应,写出反应的离子方程式:。
Ⅰ.根据下列6种符号回答问题:
①1H ② 2 H ③ 3 H ④ 14C ⑤ 14N ⑥16O
(1)共有种核素,属于种元素。
(2)互为同位素的是。(填序号,下同)
(3)质量数相等的是,中子数相等的是。
Ⅱ.现有6种物质: ①MgCl2 ②HCl ③SO2④ K2CO3 ⑤ CaO ⑥ NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是。
(2)只含离子键的化合物是。
(3)含共价键的离子化合物是。
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。已知D元素有两种常见的同素异形体,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。
(1)A元素名称是C元素在周期表中的位置。
(2)A元素的单质与水反应的离子方程式是。
(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式。该反应能否说明C元素的非金属性比B强? __(填“能”“否”)
(4)BD2和C2的水溶液均具有漂白性,二者的漂白原理————。(填“相同”或“不同”)
(5)B元素的单质在不同的条件下可以与O2发生一系列反应:
B(s) + O2(g)=BO2(g)△H =-296.8kJ·mol-1
2BO2(s) + O2(g)  2BO3(g)△H =-196.6kJ·mol-1
2BO3(g)△H =-196.6kJ·mol-1
则1 mol BO3(g)若完全分解成B(s),反应过程中的反应热DH=。