工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产ZnSO4·6H2O晶体,其工艺流程如下,有关氢氧化物沉淀时的pH如下表。
| 氢氧化物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Zn(OH)2 |
| 开始沉淀的pH |
3.3 |
1.5 |
6.5 |
5.4 |
| 沉淀完全的pH |
5.2 |
3.7 |
9.7 |
8.0 |
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 。
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是 。
为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为 。
为控制上述PH范围可选择加入的试剂或药品是 。
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是 。“操作A”的名称是 。
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于 。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+ 转变为易吸收的Fe2+,,这说明维生素C具有[(填“氧化性”或“还原性”)
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应为:S+2KNO3 +3C=K2S+N2↑+3CO2↑.该反应中还原剂是,氧化剂是。
+3C=K2S+N2↑+3CO2↑.该反应中还原剂是,氧化剂是。
有一包粉末状固体,可能是由Al2(SO4)3、CuCl2、KNO3、Na2O中的一种或几种组成的。为了探究它的成分,某学习小组做了如下实验。
①取适量粉末投入蒸馏水中,粉末完全溶解,得到蓝色透明溶液A。
②取A溶液少量,向其中逐滴滴加烧碱溶液直到过量,观察到先有沉淀出现,而后沉淀逐渐增多,然后沉淀又逐渐减少,但最终仍有部分蓝色沉淀。
③再取A溶液两份,一份滴加BaCl2溶液后,出现白色沉淀;另一份滴加硝酸银溶液后也出现白色沉淀。请回答下列问题:
(1)原白色粉末一定含有 ,一定不含,可能含有。(填化学式)
,一定不含,可能含有。(填化学式)
(2)写出过程②中涉及到的离子方程式: 。
。
(3)如果要进一步确定可能存在的物质,进行的实验操作及实验现象和结论是
。
(1)下图所示为按树状分类法对一组物质进行的分类。请填写下列标注。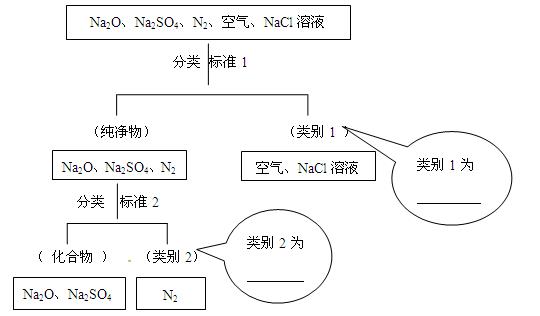
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是________________________。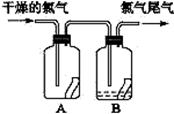
(3) 为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_________________溶液吸收多余的氯气,原理是(用化学方程式表示)__________________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是______________________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______________________(用字母代号填)。
为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_________________溶液吸收多余的氯气,原理是(用化学方程式表示)__________________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是______________________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______________________(用字母代号填)。
| A.O2 | B.Cl2 | C.CO2 | D.HClO |
(14分)莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
(1)A的分子式是。
(2)A与溴的四氯化碳溶液反应生成物的结构简式是
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是
(4)17.4克A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积(标准状况)。(5)A在浓硫酸作用下加热可得到B(B的 结构简式为
结构简式为 ),其反应类型。
),其反应类型。
(6)B的同分异构体中既含有酚羟基又含有酯基的共有种,写出其中一种同分异构体的结构简式 。
。
(10分)由乙烯和其它无机原料合成环状化合物E,请在下列图信回答下列问题:
(1)写出①的反应类型②反应条件
(2)B的结构简式 D的结构简式
D的结构简式
(3)E与氢氧化钠溶液反应的化学方程式 .