NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2 L H2O中氧原子的数目大于0.5 NA |
| B.6.0 g醋酸晶体中含有H+的数目为0.1 NA |
| C.64gCu粉与足量硫粉加热完全反应生成Cu2S时失去的电子数为2NA |
| D.1 mol Cl-含有的核外电子总数为8 NA |
根据反应式:(1)2Fe3++2I-===2Fe2++I2,(2)Br2+2Fe2+===2Fe3++2Br-,
可判断离子的还原性从强到弱的顺序是( )
| A.Br-、Fe2+、I- | B.I-、Fe2+、Br- |
| C.Br-、I-、Fe2+ | D.Fe2+、I-、Br- |
下列各组溶液中的两个反应,可用同一离子方程式表示的是( )
| A.CaCO3和HCl、Na2CO3和HCl |
| B.BaCl2和H2SO4、Ba(OH)2和H2SO4 |
| C.HNO3和K2CO3、HCl和NaHCO3 |
| D.KOH和H2SO4、Ba(OH)2和HNO3 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A.标准状况下,22.4 L H2O含有的分子数为1NA |
| B.2.4 g金属镁变为镁离子时失去的电子数为0.2NA |
| C.通常状况下,NA个CO2分子占有的体积为22.4 L |
| D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA |
下列各组离子能在溶液中大量共存的是( )
| A.Na+、Mg2+、Cl-、OH- | B.H+、Ca2+、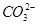 、 、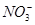 |
C.Cu2+、K+、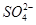 、 、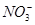 |
D.Na+、H+、OH-、Ca2+ |
下列变化需要加入某种还原剂才能实现的是( )
| A.Cl-―→Cl2 | B.H2―→HCl |
| C.CaCl2―→CaCO3 | D.Fe3+―→Fe2+ |