纯碱(化学式为Na2CO3)是一种重要的化工原料。现代化工生产有三种工艺:
一、布兰制碱法。以食盐为原料制碱,该法分三步:
①用氯化钠与硫酸反应制硫酸钠:2NaCl+H2SO4=Na2SO4+2HCl;
②用焦炭还原硫酸钠得硫化钠:Na2SO4+4C=Na2S+4CO↑
③用硫化钠与石灰石反应制碳酸钠:Na2S+CaCO3=Na2CO3+CaS
二、氨碱法即索尔维制碱法。以食盐、氨、二氧化碳为原料,其反应也分三步进行:
①NH3+CO2+H2O=NH4HCO3
②NH4HCO3+NaCl=NaHCO3+NH4Cl
③2NaHCO3=Na2CO3+CO2↑+H2O
三、候氏制碱法。低温下先向饱和食盐水中通入氨气,再通入二氧化碳可析出碳酸氢钠,再加入细盐末,因同离子效应,低温氯化铵溶解度突然降低,而食盐的溶解度变化不大,所以氯化铵析出而食盐不析出;再用氨饱和后通二氧化碳,结果往返析出NaHCO3和NH4Cl。该法生产的纯碱质量优良,纯白如雪。
(1)通过三种方法的比较,布兰制碱法工艺的缺点有 (写两点)。
(2)氨碱法工艺的中循环利用的物质是 (填化学式);产品的副产物NH4Cl既可以做氮肥又可以重新生成氨气。写出NH4Cl与生石灰反应的化学方程式 。
(3)候氏制碱法反应的方程式为 。
(4)为什么候氏制碱法工艺中先向饱和食盐水中通入氨气,再通入二氧化碳。理由是 (写两点)。
(5)候氏制碱法产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,用m1表示加热前纯碱样品的质量,m2表示加热后固体的质量。则纯碱中碳酸氢钠的质量分数可表示为: 。
卤族元素包括F、Cl、Br、I等。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 (填写序号)。
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷。
①下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为 ,
该功能陶瓷的化学式为 ;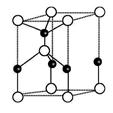
②第一电离能介于B、N之间的第二周期元素有 种。
(3)ZnCl2与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的物质的量为 。
(1)下列7种物质:
①白磷(P4) ②水晶 ③氯化铵 ④氢氧化钙 ⑤氟化钠 ⑥过氧化钠 ⑦干冰
固态时都为晶体,其中既有范德华力,又有非极性键的晶体是
(填写序号,下同),只存在离子键的是 ,熔化时只破坏
共价键的是 。
(2)下图是XeF4的结构示意图,据此判断XeF4是 (填“极性”、“非极性”)分子。
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)Z的氢化物(H2Z)与乙醇互溶,而H2Y在乙醇中溶解度较小,其原因是。
(2)Y与Z形成YZ42-的空间构型为。
(3)X与Y所形成化合物晶体的晶胞如图所示。
①在一个晶胞中,X离子的数目为;
②若该化合物的密度为ag·cm-3,则晶胞的体积是
cm3(只要求列出计算式,阿伏加德罗常数用NA表示)。
来自石油的有机化工原料A,其产量已作为衡量一个国家石油化工发展水平的标志,A可以发生如下转化: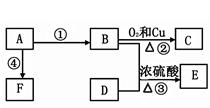
已知:E是具有果香味的有机物,其分子式为C4H8O2,F是一种高分子化合物。
(1)A的分子式是 ,C的名称是 。
(2)D分子中的官能团名称是 ,证明该官能团具有酸性的方法是 。
(3)反应③的化学方程式是;反应④的类型是反应。
短周期元素X、Y、Z、W核电荷数依次增大,X、Z同主族,Z、W同周期,四种元素的原子序数之和为37,在周期表中X是原子半径最小的元素,Y的最外层电子数是内层电子数的3倍。
(1)W在周期表中的位置是。
(2)X与Y 能形成具有18个电子的化合物,此化合物的电子式为。
(3)X、Y、Z三种元素组成的化合物中存在的化学键类型为。
(4)Z、W两种元素的最高价氧化物对应水化物溶液之间反应的离子方程式为。