下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 |
X产生氢气的体积比Y多 |
金属性:X>Y |
| B |
等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 |
HA放出的氢气多且反应速率快 |
HA酸性比HB强 |
| C |
在CuSO4溶液中加入KI溶液,再加入苯,振荡 |
有白色沉淀生成,苯层呈紫色 |
白色沉淀可能为CuI |
| D |
取久置的Na2O2粉末,向其中滴加过量的盐酸 |
产生无色气体 |
Na2O2没有变质 |
下列说法不正确的是
| A.欲提高氯水中HClO的浓度可往氯水加适量的碳酸钙粉末 |
| B.形成酸雨的氧化物主要是SO2和氮的氧化物,CO2是造成温室效应的主要气体 |
| C.氯气泄漏,自救方法是用湿毛巾或蘸有纯碱水的毛巾捂住口鼻并向地势低的地方撤离 |
| D.大气中的N2可转化为NO,NO可转化为NO2、硝酸等;含硫物质在自然界中可转化为SO2等含硫化合物 |
下列物质:①氢氟酸;②浓H2SO4;③烧碱溶液;④Na2CO3固体;⑤氧化钙;⑥浓HNO3,其中在一定条件下能与SiO2反应的有
| A.①②⑥ | B.全部 |
| C.①③④⑤ | D.②③⑥ |
甲、乙、丙、丁四种易溶于水的物质,分别由NH、Ba2+、Mg2+、H+、OH-、Cl-、HCO、SO中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1 mol·L-1乙溶液中c(H+)>0.1 mol·L-1;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论不正确的是
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42- |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
将相同质量的两块铜片分别和浓硝酸、稀硝酸(两者均过量)反应,下列叙述正确的是
| A.反应速率:两者相同 |
| B.消耗HNO3的物质的量:前者多,后者少 |
| C.反应生成气体的颜色:前者浅,后者深 |
| D.反应中转移的电子总数:前者多,后者少 |
用98%的浓硫酸(密度为1.84g/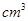 )配制100inL 1 mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,配制中使用仪器的先后顺序排列正确的是
)配制100inL 1 mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,配制中使用仪器的先后顺序排列正确的是
| A.④③⑦⑤⑥ | B.②⑤⑦⑥ | C.①③⑤⑥⑦ | D.②⑥③⑦⑤⑥ |