25 ℃时,水的电离达到平衡:H2O H++OH-,下列叙述中正确的是
H++OH-,下列叙述中正确的是
| A.将纯水加热到95 ℃时,KW变大,pH不变,水仍呈中性 |
| B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,KW变小 |
| C.向纯水中加入少量固体碳酸钠,c(H+)减小,KW不变,影响水的电离平衡 |
| D.向纯水中加入醋酸钠或盐酸,均可抑制水的电离,KW不变 |
常温常压下,将amolCO2气体通入1L1mol/L的NaOH溶液中,下列对所得溶液的描述不正确的是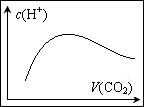
| A.当1/2<a<1时,所得溶液中一定存在: c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| B.当a=1时,所得溶液中存在: c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| C.当a=1/2时,所得溶液中存在: c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| D.当a=2时,随着CO2气体的通入,溶液中水电离出c(H+)有如上图变化关系 |
某有机物M结构如右图所示,下列说法正确的是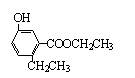
| A.1molM与足量的NaOH溶液反应,最多耗3molNaOH | |
B.M和溴水反应后所得产物的化学式为C11H12O3Br2 |
C.M分子中有7种化学环境均不同的氢原子 |
| D.M能使溴水褪色但不能使酸性高锰酸钾溶液褪色 |
下图是元素周期表中短周期的一部分,X、Y、Z、W四种元素的原子核外最外层电子数之和等于Y、Z元素的原子序数之和。下列说法正确的是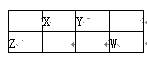
| A.X元素形成的气态氢化物分子的空间结构是三角形 |
| B.Z与Y元素形成的化合物可以是原子晶体 |
| C.W单质受热蒸发时吸收的热量用于克服共价键 |
| D.Z的最高价氧化物能溶于W的最高价氧化物的水化物中 |
下列实验方法使用不合理的是
| A.用结晶法从水溶液中获得氯化铁晶体 |
| B.用纸上层析法检验氯化铁溶液中是否混有少量氯化铜 |
| C.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量必需相等 |
| D.用AgNO3溶液、稀硝酸鉴别亚硝酸钠和食盐 |
在给定环境中,下列各组离子可以大量共存的是
| A.与铝反应放出氢气的溶液中:Na+、Mg2+、Cl-、AlO2- |
| B.滴加酚酞试液呈无色的溶液中:CO32-、K+、Na+、NO3- |
| C.在c(H+)/c(OH-)=1×1012的溶液中:NH4+、Ca2+、Cl-、K+ |
| D.pH=13的溶液中:Na+、NH4+、HCO3-、NO3- |