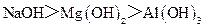有一处于平衡状态的反应:X(s)+3Y(g)  2Z(g);ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g);ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温;②低温;③高压;④低压;⑤加正催化剂;⑥分离出Z
| A.①③⑤ | B.②③⑥ | C.②③⑤ | D.②④⑥ |
实验室用Al2(SO4)3溶液制取Al(OH)3,最合适的试剂是
| A.NaOH | B.H2SO4 | C.NH3·H2O | D.KOH |
下面关于SiO2晶体网状结构的叙述正确的是
| A.存在四面体结构单元,O处于中心,Si处于4个顶角 |
| B.最小的环上,有3个Si原子和3个O原子 |
| C.最小的环上,Si和O原子数之比为1:2 |
| D.最小的环上,有6个Si原子和6个O原子 |
能正确表示下列反应的离子方程式是
A.将铜屑加入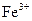 溶液中: 溶液中: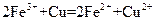 |
B.将磁性氧化铁溶于盐酸: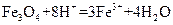 |
C.将氯化亚铁溶液和稀硝酸混合: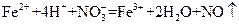 |
D.将铁粉加入稀硫酸中: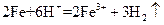 |
下列叙述中正确的是
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、Hl的稳定性依次增强 |
| D.CS2、H2O、C2H2都是直线型分子 |
下列判断错误的是
A.沸点: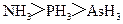 B
B .熔点:
.熔点: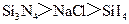
C.酸性: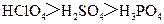 C.碱性:
C.碱性: