根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是
| 元素代号 |
A |
B |
C |
D |
E |
| 原子半径/nm |
0.186 |
0.143 |
0.089 |
0.102 |
0.074 |
| 主要化合价 |
+1 |
+3 |
+2 |
+6、-2 |
-2 |
A.最高价氧化物对应水化物的碱性A>C
B.氢化物的沸点H2D>H2E
C.单质与稀盐酸反应的速率A<B
D.C2+与A+的核外电子数相等
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生气泡的是( )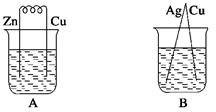
茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、PtFe合金网为电极材料的海水电池。在这种电池中( )
①铝合金是正极 ②铝合金是负极 ③海水是电解液 ④铝合金电极发生还原反应
| A.②③ | B.②④ | C.①② | D.①④ |
下面是四个化学反应,你认为理论上不可用于设计原电池的化学反应是( )
| A.Zn+Ag2O+H2O===Zn(OH)2+2Ag |
| B.Pb+PbO2+2H2SO4===2PbSO4+2H2O |
| C.Zn+CuSO4===Cu+ZnSO4 |
D.C+CO2 2CO 2CO |
对于原电池的电极名称叙述有错误的是( )
| A.发生氧化反应的为负极 |
| B.正极为电子流入的一极 |
| C.比较不活泼的金属为负极 |
| D.电流的方向由正极到负极 |
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述中不正确的是( )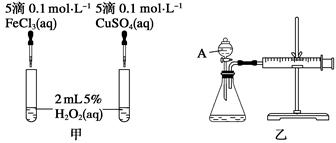
| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图甲所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 |
| C.用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查图乙所示装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |