一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收。用下图装置加热硫酸铜粉末直至完全分解。若硫酸铜粉末质量为10.0 g,完全分解后,各装置的质量变化关系如下表所示。
| 装置 |
A(试管+粉末) |
B |
C |
| 反应前 |
42.0 g |
75.0 g |
140.0 g |
| 反应后 |
37.0 g |
79.5 g |
140.0 g |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是
A.4CuSO4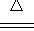 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑
B.3CuSO4 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑
C.5CuSO4 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑
D.6CuSO4 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
有NaCl、NH4Cl、AlCl3、CuCl2、Na2SO4五种溶液,只用一种试剂把它们鉴别开来,该试剂是
| A.盐酸 | B.烧碱溶液 |
| C.氯化钡溶液 | D.氢氧化钡溶液 |
下列溶液与100 mL 0.5 mol/L NaCl溶液中所含的Cl-物质的量浓度相同的是
| A.100 mL 0.5 mol/L MgCl2溶液 | B.200 mL 0.25 mol/L AlCl3溶液 |
| C.50 mL 1 mol/L NaCl溶液 | D.25 mL 0.5 mol/L HCl溶液 |
下列物质在水溶液中的电离方程式错误的是
A.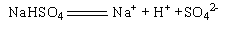 |
B.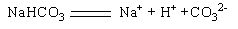 |
C.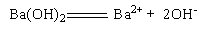 |
D. |
实验室里不同化学试剂的保存方法不尽相同,①NaOH溶液 ②大理石 ③NaCl溶液 ④稀硝酸4种试剂通常各自存放在如下图所示的玻璃试剂瓶中。按照试剂瓶的顺序存放试剂序号正确的是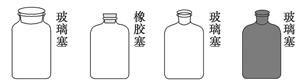
| A.①②③④ | B.②①④③ | C.②③④① | D.②①③④ |
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
| A.分液、蒸馏、萃取 | B.萃取、蒸馏、分液 |
| C.分液、萃取、蒸馏 | D.蒸馏、萃取、分液 |