现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、 、
、 、X中的一种。
、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是________和________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X为________(填字母)。
A.Br- B.
C.CH3COO- D.
(3)将19.2 g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式:________________,若要将Cu完全溶解,至少加入H2SO4的物质的量是________。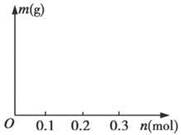
(4)若用惰性电极电解C和D的混合溶液,溶质的物质的量均为0.1 mol,请在坐标系中画出通电后阴极析出固体的质量m与通过电子的物质的量n的关系。(标明纵坐标数值)
(5)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为______________________________。
H2S在水中的电离方程式为。
(1)向H2S溶液中加入浓盐酸时,电离平衡向(填左、右、不)移动,c(H+)(填增大、减小、不变),c(S2-)(填增大、减小、不变)。
(2)向H2S溶液中加入NaOH固体,电离平衡向(填左、右、不)移动,c(H+)(填增大、减小、不变),c(S2-)(填增大、减小、不变)。
(3)若要使H2S溶液中c(HS-)增大,且使H2S的电离平衡逆向移动,可以加入。
(4)向H2S溶液中加水,c(HS-)(填增大、减小、不变),溶液pH(填增大、减小、不变)
互为同分异构体的有机物A、B、C的分子式均为C5H8O2,其中A为直链结构,加热时能与新制的氢氧化铜浊液反应,生成砖红色物质;A分子中核磁共振氢谱图中有三组峰,且峰面积之比为2:1:1。B为五元环酯。C的红外光谱表明其分子中存在甲基。A~I等有机物的转化关系如下:
已知:烯烃在一定条件下可与卤素单质发生a—H原子的取代反应。
(1)A、B的结构简式分别是:A,B。
(2)C为反式结构,其结构式为。
(3)写出下列反应的化学方程式;
D→C:。
G→H:。
(4)写出下列反应类型:
F→G,A→I中的①。
(5)写出F发生加聚反应生成的产物的结构简式。
(6)与A的官能团组成和个数均相同的同分异构体
还有个。
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/LKOH溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系正确的是
| A.c =" 1000b" / (22.4V) | B.p=" m+" Vc / 125 | C.n =" m" +17 Vc | D.5/3 <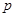 <17/ 9 <17/ 9 |
脱水偶联反应是一种新型的直接烷基化反应,例如:
(1)化合物Ⅰ的分子式为,1mol该物质完全燃烧最少需要消耗molO2。
(2)化合物Ⅱ可使溶液(限写一种)褪色;以化合物Ⅱ为原料可制备高分子化合物,其结构简式是;化合物Ⅲ(分子式为C10H11C1)可与NaOH水溶液共热生成化合物Ⅱ,相应的化学方程式为。
(3)化合物Ⅲ与NaOH乙醇溶液共热生成化合物Ⅳ,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为1:1:1:2,Ⅳ的结构简式为。
(4)由CH3COOCH2CH3可合成化合物Ⅰ。化合物Ⅴ是CH3COOCH2CH3的一种无支链同分异构体,碳链两端呈对称结构,且在Cu催化下与过量O2反应生成能发生银镜反应的化合物Ⅵ。Ⅴ的结构简式为,Ⅵ的结构简式为。
(5)一定条件下, 也可以发生类似反应①的反应,有机产物的结构简式为。
也可以发生类似反应①的反应,有机产物的结构简式为。
X、Y、Z、W是元素周期表中前30号元素,且原子序数依次增大。其相关信息如下表:
| 元素 |
相关信息 |
| X |
X原子基态时最外层电子数是其内层电子总数的2倍 |
| Y |
Y的基态原子最外层电子排布式为nsnnpn+2 |
| Z |
Z元素的最高正价与负价代数和为6 |
| W |
W基态原子未成对电子数是前30号元素中最多的 |
(1)W位于元素周期表第周期第族,其基态原子最外层有个电子。
(2)X的第一电离能比Y的(填“大”或“小”),1mol X22-中含有的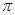 键数目为。
键数目为。
(3)X和Y的气态氢化物中,较稳定的是(写化学式),Y的同族元素(包括Y)的最简单氢化物中沸点最低的是。
(4)写出KZY3与HZ浓溶液反应制取Z2的化学方程式,并标出电子转移的方向和数目
。
(5)已知:X(s)+Y2(g)=XY2(g) ΔH 1= -393.5 kJ•mol-1
XY(g) +1/2Y2(g)=XY2(g) ΔH 2= -282.9 kJ•mol-1
则X(s)与Y2(g)反应生成XY(g)的热化学反应方程式为。