氨水是一种的常用的化学试剂。
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少 量氨气。已知:NH3·H2O+CaO=Ca(OH)2+NH3↑。
①生石灰应该装在 (填A或B)。
②试从电离平衡角度分析该实验中氨气逸出的原因: 。
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二: 。
②你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、 0.25mol/L NaOH溶液、盐酸 、 2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验步骤 |
实验操作 |
预期现象及结论(步骤1只填现象) |
| 1 |
在A、B两支洁净的试管中各入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液。 |
|
| 2 |
|
|
(3)吸取20.00ml 上述氨水于锥形瓶,滴加3滴甲基橙指示剂,用0.0050mol/L标准硫酸滴定,滴定至出现红色为终点,重复3次实验,平均消耗标准硫酸20.04 ml,计算上述氨水的物质的量浓度
(16分)已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性。
Ⅰ.用如上图所示装置进行Mg和SO2的实验,其中A是制备SO2的发生装置。
⑴选择制取SO2的合适试剂____________。(填序号)
①10%的H2SO4溶液②80%的H2SO4溶液 ③Na2SO3固体④CaSO3固体
⑵写出装置B中发生的主要反应的化学方程式_______________________________。装置C中NaOH溶液的作用是 。
⑶请画出制备SO2的发生装置并注明主要仪器的名称,固定仪器省略不画。
(4)你认为该装置不足之处是什么?
Ⅱ.某研究性学习小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si ②Mg在点燃的条件下即可与SiO2反应
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4 ④Si和SiO2均不与稀H2SO4反应
⑤SiH4在空气中自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
⑸该小组“实验室制Si”的化学方程式是_____________________________。
(6)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是____。
实验题
Ⅰ以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。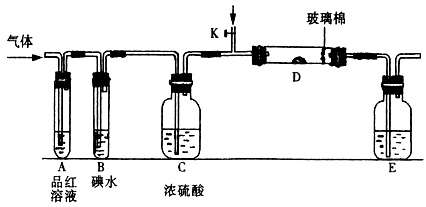
若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?(填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为。
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为。
(2) 某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母),仍然无法观察到沉淀产生。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成–2价酸根离子X,X中S和O的质量比为2∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式。
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图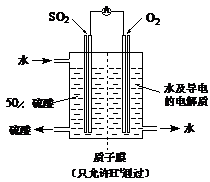
含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为_________极,其电极反应式为;电池的总反应式
Ⅱ实验是化学研究的基础,关于下列各装置图的叙述正确的是(填序号)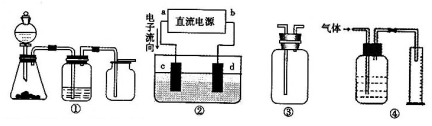
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正极,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是(填序号)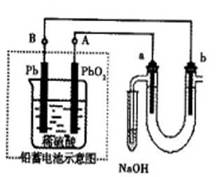
A.铅蓄电池负极的反应式为:Pb—2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
(12分)用中和滴定法测定某烧碱样品的纯度。有以下步骤:
(1)配制待测液:用5.00 g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000 mL溶液。除烧杯、胶头滴管、玻璃棒外,还需要的玻璃仪器有___。
(2)滴定:
①盛装0.1000 mol·L-1盐酸标准液应该使用_________式滴定管。
②滴定时眼睛应。
③有关数据记录如下:
| 测定序号 |
待测溶液的体积/mL |
所耗盐酸标准液的体积/mL |
|
| 滴定前 |
滴定后 |
||
| 1 |
20.00 |
0.50 |
20.78 |
| 2 |
20.00 |
1.20 |
21.32 |
(3)计算:烧碱样品的纯度是_________________。
(4)误差分析(选填“偏高”“偏低”或“无影响”):
①用蒸馏水冲洗锥形瓶,则会使测定结果___________;
②读数时,滴定前仰视,滴定后俯视,则会使测定结果___________。
下列物质A~F是我们熟悉的单质或化合物,其中A、B是常见的金属,E在常温下是黄绿色气体;在适当的条件下,他们之间可以发生如图所示的转化。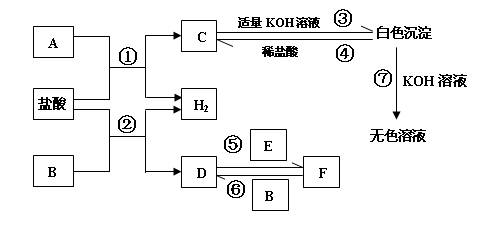
试回答下列问题:
(1)A的化学式是;
(2)在①—⑦反应中,属于氧化还原反应的有,其中属于置换反应的有;
(3)写出上图中白色沉淀与NaOH溶液反应的离子方程式:
;
(4)请写出在D的溶液中滴加NaOH溶液的过程中发生反应的化学方程式
、
。
(5)检验上图无色溶液中金属阳离子的方法是(填写实验名称):,
现象是。
某学生课外活动小组利用右图所示装置分别做如下实验: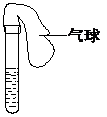
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后又恢复红色,则原溶液可能是(只填一种)
加热时溶液由红色逐渐变浅的原因是:
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是(只填一种)______;加热时溶液由无色变为红色的原因是 。