工业碳酸钠(纯度约为98%)中含有Mg2+、Fe2+、Cl-和SO42-等杂质,提纯工艺流程如下:
已知:碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
回答下列问题:
(1)溶解时通入热空气的作用有 (写出两条即可);生成氢氧化镁沉淀的离子方程式为 。
(2)“趁热过滤”时的温度应控制在 ;简述过滤后洗涤固体的操作 。
(3)为检验母液中是否含有Cl-,必须加入的试剂为 。
(4)实验室进行“灼烧”的陶瓷仪器有 。
(5)室温下用石墨电极电解饱和Na2CO3溶液(装置如图),写出Y电极反应式: ;一段时间后X电极可收集到的气体一定有 ,可能有 。
A为只含有C、H、O三种元素的芳香烃衍生物,各物质间的相互转化关系如下图。已知:ROH+HX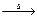 RX+H2O;E为加聚得到的高分子化合物,分子式为(C9H8O2)n;I中除含有一个苯环外还含有一个六元环,分子式为C9H8O2;H分子式为C18H16O6。
RX+H2O;E为加聚得到的高分子化合物,分子式为(C9H8O2)n;I中除含有一个苯环外还含有一个六元环,分子式为C9H8O2;H分子式为C18H16O6。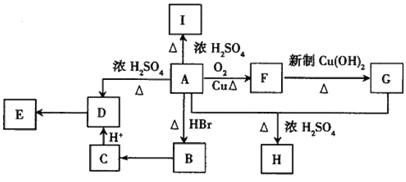
(1)写出A、E、I的结构简式:A;E;I。
(2)B→C的反应条件为____________________。
(3)A+G→H的反应类型为。
(4)有机物A的同分异构体只有两个对位取代基,既能与Fe3+发生显色反应,又能发生水解反应,但不能发生银镜反应。则此类A的同分异构体有4种。例如:
请写出另两种同分异构体。
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。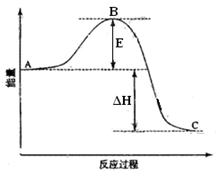
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99kJ·mol-1。请回答下列问题: (1)图中A、C分别表示、,E的大小对该反应的反应热有无影响?。该反应通常用V2O5作催化剂加快速率,加V2O5会使图中B点升高还是降低?,理由是;
(1)图中A、C分别表示、,E的大小对该反应的反应热有无影响?。该反应通常用V2O5作催化剂加快速率,加V2O5会使图中B点升高还是降低?,理由是; (2)图中△H=kJ·mol-1;
(2)图中△H=kJ·mol-1; (3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式; (4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 molSO3(g)的△H=。
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 molSO3(g)的△H=。
研究有机物一般经过以下几个基本步骤:分离、提纯 → 确定实验式 → 确定分子式 → 确定结构式。有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。
为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为。 |
| (2)将此9.0gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
(2)A的分子式为。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)写出A中含有的官能团的名称 。 |
(4)A的核磁共振氢谱如下图: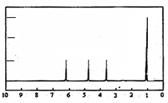 |
(4)A中含有种氢原子。 综上所述, A的结构简式为。 |
工业上利用焦炭在石灰窑中燃烧放热,使石灰石分解生产CO2。主要反应如下:
C+O2→CO2①, CaCO3→CO2↑+CaO②
(1)含碳酸钙95%的石灰石2.0 t按②完全分解(设 杂质不分解),可得标准状况下CO2的体积为_______
杂质不分解),可得标准状况下CO2的体积为_______ __________m3。
__________m3。
(2)纯净的CaCO3和焦炭混合物m g在石灰窑中完全反应,所得CO2的物质的量范围是_______________________。
(3)纯净的CaCO3和焦炭按①②完全反应,当窑内配比率
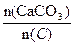 =2.2时,窑气中CO2的最大体积分数为多少?(设空气只含N2与O2,且体积比为4∶1,下同)
=2.2时,窑气中CO2的最大体积分数为多少?(设空气只含N2与O2,且体积比为4∶1,下同)
(4)某次窑气成分如下:O2 0.2%,CO 0.2%,CO2 41.6%,其余为N2。则此次窑内配比率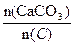 为何值?
为何值?
将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
(1)写出OA段所发生反应的离子方程式_______________________________、
______________。
(2)当加入35mL盐酸时,产生CO2的体积为___________mL(标准状况)。
(3)计算原混合物中碳酸钠、碳酸氢钠共_____________mol。