用①质子数、②中子数、③电子数、④质量数、⑤同位素填空,
请将序号填在后面横线上。
(1)136C与147N具有相同的 ,(2)136C与126C具有相同的 ,
(3)146C与147N具有相同的 ,(4)157N与147N互为 。
已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75% ,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为无色液体。反应生成的水均已略去。它们有如下图所示的关系。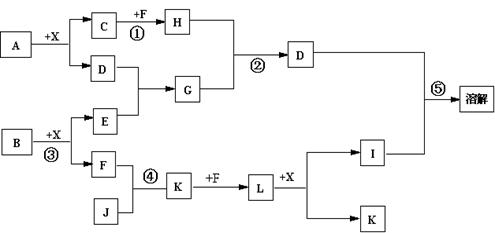
(1)写出化学式:A B J 。
(2)反应③中每生成1molF,转移电子的数目为:。
(3)反应④的化学方程式为:。
(4)离子方程式分别为:反应② ;
⑤ 。
(5)反应①中,每1.00gC与足量的F作用,恢复到25oC放出55.6kJ热量,写出反应①的热化学方程式 。
写出C6H14主链上有4个碳原子的所有的同分异构体
(每空1分,共11分)写出有关离子方程式
(1)Na2SO4溶液中滴加Ba(OH)2:
(2)H2S的电离方程:
(3)NH4Cl溶液显性:
(4)纯碱溶液显性:
(5)将FeCl3饱和溶液滴入沸水中:
(6)用明矾净水:
(7)在配制AlCl3溶液时,为了防止发生水解,可以加入少量的;在配制FeSO4溶液时,为了防止溶液变质,可以加入少量的和。
(每空2分,共8分)
(1)用系统命名法给烷烃 命名:
命名:
(2)写出些列有关化学方程式
①实验室制取乙炔:
②乙烯通入溴水中:
3有乙烯制取聚乙烯:
氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)氢气是清洁能源,其燃烧产物为。
(2)
是一种重要的储氢载体,能与水反应达到
,且反应前后
的化合价不变,该反应的化学方程式为,反应消耗1
时转移的电子数目为。
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢: 。某温度下,向恒容密闭容器中加入环己烷,起始浓度为
,平衡时苯的浓度为
,该反应的平衡常数
=。
。某温度下,向恒容密闭容器中加入环己烷,起始浓度为
,平衡时苯的浓度为
,该反应的平衡常数
=。
(4)一定条件下,题11图示装置可实现有机物的电化学储氢(忽略其它有机物)。
①导线中电子移动方向为。
②生成目标产物的电极反应式为
③该储氢装置的电流效率 =(
=( =
= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)