硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:
已知某些氢氧化物沉淀的pH如下表所示:
| 氢氧化物 |
开始沉淀时的pH |
完全沉淀时的pH |
| Mg(OH)2 |
9.3 |
10.8 |
| Fe(OH)2 |
7.6 |
9.6 |
| Fe(OH)3 Al(OH)3 |
2.7 3.7 |
3.7 4.7 |
(1)MgO的电子式为 。
(2)滤渣2的主要成分是 ,向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为 。
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为 (用含有a、b的代数式表示)。
元素X位于IA族,原子核内没有中子,Y元素原子的原子核外有9个电子,X与Y能形成稳定化合物,该化合物的化学式是________,它是通过___ _____键结合的,用电子式表示它的形成过程:。
A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。A、B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol·L—1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。 C的最高价氧化物的水化物是所有含氧酸中酸性最强的;D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的水化物的化学式为____________。
(2)A元素是_______,B元素是______,D元素是______。(写元素符号)
(3)A与D形成的原子个数比为2:1的化合物的化学式是___ _ ____,
用电子式表示它的形成过程
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,
其离子方程式为______________________________ __________________。
1mol某烃A和1 mol苯完全燃烧,烃A比苯多消耗1mol O2,若A分子结构中无支链或侧链,则:(1)若A为环状化合物,它能与等物质的量的Br2发生加成反应,则A的结构简式为;
(2)若A为链状烯烃,1mol A最多可和2mol Br2发生加成反应且A与等物质的量的Br2加成后的可能产物只有2种,则A的结构简式为。
有机物的结构可用“键线式”简化表示。CH3—CH=CH-CH3可简写为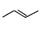 。
。
有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式:
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有种。
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
(1)正四面体烷的分子式为,其二氯取代产物有种
(2)关于乙烯基乙炔分子的说法错误的是:
a.能使酸性KMnO4溶液褪色
b.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):
、。