【化学一选修2:化学与技术】(15分)
利用硫酸工业废渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,②__________________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO ,该反应的离子方程式为____________.
,该反应的离子方程式为____________.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。
实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-===2Fe2++SnCl
Sn2++4Cl-+2HgCl2="==" SnCl +Hg2Cl2↓
+Hg2Cl2↓
6Fe2++ Cr2O +14H+===6Fe3++2Cr3++7H2O
+14H+===6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量__________(填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量偏高,其原因是_____________。
(4)①可选用______________(填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是_________________(用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的,pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Al(OH)3 |
Mg(OH)2 |
Mn(OH)2 |
| 开始沉淀 |
2.3 |
7.5 |
3.4 |
9.4 |
8.3 |
| 完全沉淀 |
3.2 |
9.7 |
4.4 |
12.4 |
9.8 |
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:________________________________;b.沉淀:_____________________________;
c.分离,洗涤;d.烘干,研磨。
弱电解质的电离平衡、盐类的水解平衡和难溶电解质的溶解平衡均属于化学学习中的动态平衡。已知H2A在水中存在以下平衡:H2A H++HA-,HA-
H++HA-,HA- H++A2-。
H++A2-。
(1)Na2A溶液显碱性的原因 (用离子方程式回答);
(2)某温度下,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1 mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是 。
A.c(H+)·c(OH-)=1×10―14B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)D.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s) Ca2+(aq)+A2-(aq) △H>0。 Ksp=C(Ca2+)·C(A2—)
Ca2+(aq)+A2-(aq) △H>0。 Ksp=C(Ca2+)·C(A2—)
①降低温度时,Ksp (填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,C(Ca2+) ,原因是 ;
(4)CaCO3是一种难溶物质,其Ksp=2.8×10—9,CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为 。
[化学——选修3:物质结构与性质]
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)+3价Cr的配合物K[Cr(C2O4)2(H2O)2]中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。
(2)CaO晶胞如图所示,与每一个钙离子距离最近并且距离相等的钙离子有_________个 ;CaO晶体和NaCl晶体的晶格能分别为:CaO:3401 kJ/mol、NaCl:786 kJ/mol。 导致两者晶格能差异的主要原因__________________。
(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键类型是__________,则形成的化学键类型是 。
(4)从不同角度观察MoS2的晶体结构见图。已知:Mo位于第五周 期VIB族。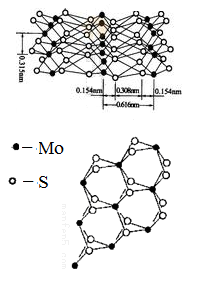
①下列说法正确的是__________
| A.晶体硅中硅原子的轨道杂化类型为sp2 |
| B.电负性:C<S |
| C.晶体硅和C60比较,熔点较高的是C60 |
| D.Mo元素基态原子的价电子排布式为4d55s1 |
E.MoS2的晶体中每个Mo原子周围距离最近的S原子数目为4
F.MoS2的晶体中Mo-S之间的化学键为极性键、配位键、范德华力
②根据MoS2的晶体结构回答:MoS2纳米粒子具有优异的润滑性能,其原因是_____________ .
[化学——选修2:化学与技术]
海水资源丰富,海水中主要含有 等离子。合理利用海水资源和保护环境是我国可持续发展的重要保证。
等离子。合理利用海水资源和保护环境是我国可持续发展的重要保证。
Ⅰ.火力发电燃煤排放的 会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
(1)天然海水的pH≈8,呈弱碱性。用离子方程式解释原因 。
(2)天然海水吸收了含硫烟气后,要用 进行氧化处理,氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是___________________。
进行氧化处理,氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是___________________。
Ⅱ.重金属离子对河流及海洋造成严重污染。某化工厂废水(pH=2.O,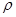 ≈1g·mL-1)中含有
≈1g·mL-1)中含有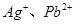 等重金属离子,其浓度各约为0.01mol·L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:
等重金属离子,其浓度各约为0.01mol·L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 |
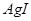 |
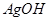 |
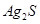 |
 |
 |
 |
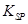 |
8.3×10-17 |
5.6×10-8 |
6.3×10-50 |
7.1×10-9 |
1.2×10-15 |
3.4×10-28 |
(3)你认为往废水中投入__________(填字母序号),沉淀效果最好。
A. B.
B.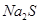 C.
C. D.
D.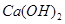
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中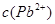 =__________。
=__________。
(5)如果用食盐处理其只含 的废水,测得处理后废水中
的废水,测得处理后废水中 的质量分数为0.117﹪。
的质量分数为0.117﹪。
若环境要求排放标准为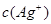 低于1.O×lO-8mol·L-1,问该工厂处理后的废水中
低于1.O×lO-8mol·L-1,问该工厂处理后的废水中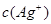 =__________。已知
=__________。已知 =1.8×l-10mol2·L2。
=1.8×l-10mol2·L2。
金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,转化关系如下:
已知:气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。
请回答下列问题
(1)A和B两溶液混合产生白色沉淀,产生该沉淀的离子反应方程式为 。
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质的电子式 。
(3)完成并配平下列离子方程式:Al+NO3-+OH-+H2O——__ + 。
(4)Al与NO3-在酸性条件下反应,Al与被还原的NO3-的物质的量之比是 。
《物质结构与性质》
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)Fe基态原子核外电子排布式为 。
(2)H、N、O的电负性从小到大的顺序是 。
(3)与NO2+互为等电子体的一种分子为 (填化学式)。
氨基(-NH2)中氮原子的杂化类型为 。
(4)1mol乙酸分子中含有σ键的数目为 。
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为 。