反应N2O4(g)  2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是 ( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是 ( )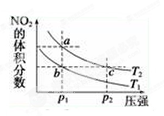
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深,c浅 |
| C.b、c两点的平衡常数:b<c |
| D.a、c两点气体的平均相对分子质量:a>c |
分子式为C10H14的二取代芳香烃,其可能的结构有
| A.3种 | B.6种 | C.7种 | D.9种 |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.往沸水中滴加0.1molFeCl3饱和溶液,制得的胶体中含0.1NA个Fe(OH)3胶体粒 |
| B.标准状况下,11.2L C2H6含3NA个C—H极性共价键 |
| C.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5 NA |
| D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
下列叙述中正确的是
| A.干燥的Cl2和氯水均能使鲜花褪色 |
| B.向碘水中通入SO2,碘水褪色说明SO2具有漂白性 |
| C.向FeBr2溶液中滴加少量氯水,溶液变浅黄色是因为生成了Br2 |
| D.将Cl2通入AgNO3溶液中不会有沉淀产生 |
化学是一门中心学科,与社会发展的需要有密切的关系。下列说法中,不正确的是
| A.用食醋可除去热水壶内壁的水垢 |
| B.合成纤维和光导纤维都是新型无机非金属材料 |
| C.酒精能使蛋白质变性,可用于杀菌消毒 |
| D.白酒用于增稠增香的塑化剂邻苯二甲酸二丁酯不溶于水,有毒 |
一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应如下:2A(g)+B(s) 2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
| 实验Ⅰ |
实验Ⅱ |
实验Ⅲ |
|
| 反应温度/℃ |
800 |
800 |
850 |
| c(A)起始/mol·L-1 |
1 |
2 |
1 |
| c(A)平衡/mol·L-1 |
.0.5 |
1 |
0.85 |
| 放出的热量/kJ |
a |
b |
c |
A.实验III的化学平衡常数K<1
B.实验放出的热量关系为b>2a
C.实验III在30min达到平衡时的速率v(A)为0.005mol• L-1·min-1
D.当容器内气体密度不随时间而变化时上述反应达到平衡