工业生产的氢氧化钠常含有碳酸钠杂质。为测定某样品中氢氧化钠纯度,设计以下实验。(装置气密性良好,每一步骤反应完全,浓H2SO4具有吸水性)
【实验设计】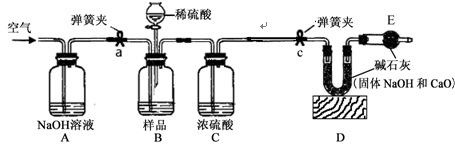
【实验过程】
(1)打开弹簧夹a,先对装置A、B、C(已连接)通入空气一会儿,以排尽装置含有的 ,再关闭弹簧夹a,接上装置D和E,打开弹簧夹c,把硫酸滴入样品中。
(2)反应结束后,待装置冷却后直接称量装置 (填字母序号)。根据该装置在反应前后的质量差得到CO2的质量,由此计算出该样品中碳酸钠的质量,最后得到样品中氢氧化钠纯度。
【数据分析】
最后计算得到样品中氢氧化钠纯度比实际数据偏大,反思整个实验过程,造成误差可能的原因 。
化学就在我们身边,它能改善我们的生活。请从①活性炭②一氧化碳③甲烷④小苏打⑤熟石灰⑥钛合金中选择适当物质的序号填空
(1)发酵粉可以使食品松软可口,属于发酵粉成分之一的是;
(2)常用来改良酸性土壤的碱是;
(3)可用来除去冰箱异味的是;
(4)天然气、沼气中的主要成分;
(5)吸烟对人体有害。燃着的香烟产生的烟气中含有一种能与血液中血红蛋白结合的有毒气体,它是;
(6)可制造人造骨的是。
如果不小心将浓硫酸弄到皮肤上,应该。
①二个氮气分子;②三个硫酸根离子;③石灰石的主要成分
按下列要求书写化学方程式:
⑴细铁丝在纯氧中燃烧;
⑵高温煅烧石灰石;
⑶铁粉加入稀盐酸溶液中。
将3g碳和6g氧气放入一密闭容器中.点火燃烧后,容器中的气体为________(填纯净物”或“混合物”);当恢复到原温度时,容器内的压强_____(填“增大”、“减小”、“不变”)