已知热化学方程式N2(g) + 3H2(g)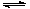 2NH3(g) + Q kJ(Q>0),下列说法中,正确的是
2NH3(g) + Q kJ(Q>0),下列说法中,正确的是
| A.1mol N2(g)和3mol H2(g)具有的能量之和低于2 mol NH3(g)具有的能量 |
| B.将1mol N2 (g)和3mol H2 (g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| C.升高温度,平衡向逆反应方向移动,上述热化学方程式中的Q值减小 |
| D.将一定量N2(g)和H2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有3mol H2被氧化 |
一定温度下,用蒸馏水稀释0.1 mol·L-1的氨水,则在稀释过程中,下列各数值保持增加趋势的是()
A.c(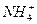 ) ) |
B.c(NH3·H2O) |
| C.c(OH-) | D.c(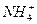 )与c(NH3·H2O)的比值 )与c(NH3·H2O)的比值 |
下列各组数据关系,前者比后者大的是()
| A.纯水100 ℃和25 ℃时的pH |
| B.0.1 mol·L-1的盐酸与0.1 mol·L-1的醋酸的pH |
| C.100 mL 0.1 mol·L-1的CH3COOH溶液与10 mL 0.1 mol·L-1的CH3COOH溶液中的H+数目 |
D.0.1 mol·L-1的氨水中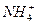 浓度与OH-浓度 浓度与OH-浓度 |
把1 mL 0.1 mol·L-1的H2SO4加水稀释制成2 L溶液,在此溶液中由水电离产生的H+浓度接近于()
| A.1×10-4mol·L-1 | B.1×10-8mol·L-1 | C.1×10-11mol·L-1 | D.1×10-10mol·L-1 |
60 mL 0.5 mol·L-1氢氧化钠溶液和40 mL 0.4 mol·L-1硫酸混合后溶液的pH约为()
| A.0.5 | B.1.7 | C.2 | D.13.2 |
25 ℃时,0.1 mol·L-1的盐酸中,水的离子积为()
| A.1×10-13 | B.1×10-15 | C.1×10-14 | D.5×10-12 |