已知A、B、C、D、E、F六种短周期元素中,A、B、C、D是组成蛋白质的基本元素;A与B的原子序数之和等于C原子核内的质子数;A与E、D与F分别位于同一主族,且F原子核内的质子数是D原子核外电子数的2倍。据此,请回答:
(1)F在周期表中的位置是 。
(2)由A、C、D、F按8:2:4:1原子个数比组成的化合物甲中含有的化学键类型为 ;甲溶液中各离子浓度由大到小的顺序为 (用离子浓度符号表示)。
(3)化合物乙由A、C组成且相对分子质量为32;化合物丙由A、D组成且分子内电子总数与乙分子内电子总数相等;乙与丙的反应可用于火箭发射(反应产物不污染大气),则该反应的化学方程式为 。
(4)由A、D、E、F组成的化合物丁能与硫酸反应并放出刺激性气味的气体,则丁的化学式为 ;实验测得丁溶液显弱酸性,由此你能得出的结论是 。
(5)由B、A按1:4原子个数比组成的化合物戊与D的常见气态单质及NaOH溶液构成原电池(如图),试分析: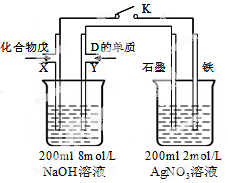
①闭合K,写出左池X电极的反应式 ;
②闭合K,当X电极消耗1.6g化合物戊时(假设过程中无任何损失),则右池两极共放出气体在标准状况下的体积为 升。
在标准状况下,18 g CO和CO2的混合气体完全燃烧后得到11.2 L CO2。则原混合气体的密度是_______________;原混合气体中,CO的质量是______________g,CO2的体积是______________,碳原子和氧原子的个数比为______________。
许多物质的氧化能力受溶液酸碱性的影响。高锰酸钾在不同条件下发生的还原反应如下:
①酸性:MnO4-+5e-+8H+→Mn2++4H2O;
②中性:MnO4-+3e-+2H2O→MnO2+4OH-
③碱性:MnO4-+e-→MnO42-(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H++2e-→Mn2++2H2O
(1)MnO2与稀盐酸不能制取氯气,其原因是___________________________________。
(2)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列叙述正确的是_______。(选填编号)
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(3)写出将SO2通入KMnO4溶液中所发生反应的离子方程式,并配平:
________________________________________________________________________。
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,已知产物中K2SO4和S的物质的量之比为3∶2。完成并配平该反应的化学方程式:
□KMnO4+□K2S+□__________→□K2MnO4+□K2SO4+□S↓+□__________,反应若生成5.44 g硫单质,反应过程中转移电子的物质的量为__________________。
铜(Cu)是重要金属,铜的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)向CuSO4浓溶液中滴入浓氨水,直至产生的沉淀恰好溶解,可得到深蓝色的透明溶液。再向其中加入适量乙醇,可析出深蓝色的Cu(NH3)4SO4•H2O晶体。
①沉淀溶解的离子方程式为_______________________________________________。
②乙醇的作用是_________________________________________________________。
③[Cu(NH3)4]2+具有对称的立体构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的立体构型为____________________,其中N原子的杂化轨道类型是________。
(2)金(Au)与铜为同族元素,铜与金可形成具有储氢功能的合金。
①合金中,原子间的作用力是_______________。已知Au为第六周期元素,则基态Au原子的价电子排布式为________,Au的原子序数为________。
②该储氢合金为立方最密堆积结构,晶胞中Cu原子位于面心、Au原子位于顶点,储氢时,H原子进入由Cu原子与Au原子构成的四面体空隙中,则该晶体储氢后的化学式为_______________。
水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)在酸性溶液中,水分子容易得到一个H+,形成水合氢离子(H3O+)。对于这一过程,下列描述不合理的是______________。
| A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
根据价层电子对互斥理论推测H3O+的形状为_____________________。
(2)水分子和硫化氢分子的键角及中心原子的杂化方式如下表:
| 分子 |
H2O |
H2S |
| 中心原子杂化方式 |
sp3 |
|
| 键角 |
104.5° |
92.1° |
| 键长 |
95.7 pm |
133.6 pm |
根据表格中的数据判断O-H键键能______(填“>”、“=”或“<”)S-H键键能。用电负性知识解释H2O的键角大于H2S的键角的原因:________________________
__________________________________________________________。
(3)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是________kJ/mol。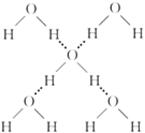
某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色。在一定条件下,它们有如下的转化关系(无机物已略去)。其中,G能与NaHCO3溶液反应,H不能与新制Cu(OH)2反应,J分子内有两个互为对位的取代基。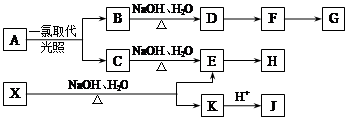
(1)A物质的名称为________________。写出所有属于芳香烃的A的同分异构体的结构简式__________________________________________________________________。
(2)J中所含的含氧官能团的名称为_____________________________________。
(3)E与G反应的化学方程式是________________________,反应类型是__________。
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的名称是_______________。
(5)已知J有多种同分异构体,写出符合下列性质的J的同分异构体的结构简式:
①与FeCl3溶液作用显紫色;
②与新制Cu(OH)2悬浊液作用产生砖红色沉淀;
③苯环上的一卤代物有2种。
____________________________________________________________。