0.2 mol有机物和0.4 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8 g;再通过灼热CuO充分反应后,固体质量减轻3.2 g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6 g。
(1)判断该有机物的化学式。
(2)若0.1 mol该有机物恰好与4.6 g金属钠完全反应,试确定该有机物的结构简式。(已知:一个碳上接两个羟基是不稳定的)
用系统命名法命名下列有机物:
(1)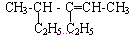 ________________________
________________________
(2)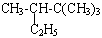 ______________________________________________
______________________________________________
(1)键线式 表示的分子式 ;名称是 。
表示的分子式 ;名称是 。
(2)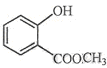 中含有的官能团的名称为 。
中含有的官能团的名称为 。
(3)丁基的4个结构简式为_ 。
用下图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。
(1)A中发生反应的化学方程式为_________________________________。
(2)在B中观察到的现象是______________________________________。
(3)室温下,若从电解开始到时间t s,A、B装置中共收集到气体0.168 L(标准状况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1 000 mL,则A溶液的pH为__________________。
在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按下图连接。
(1)如果把电键K接A,该装置应是________,Zn①为________极,Zn②的电极反应为________________。
(2)上述反应进行5 min后,转换电键K到B,则这一装置是________,Zn②为________极,Zn①的电极反应式是____________________。
(3)将Zn②换成铁片,电解质溶液换成ZnCl2饱和溶液,K接A,此时该装置为______池,阴极电极反应式为____________________________。
氯铝电池是一种新型的燃料电池,电解质溶液是KOH溶液。试回答下列问题:
(1)通入氯气的电极是__________极(填“正”或“负”);
(2)铝电极是__________极(填“正”或“负”);
(3)电子从__________(填“Al”或“Cl2”,下同)电极流向__________的电极。